- 詳細
コンゴ民主共和国におけるクレードI によるエムポックスの流行について
2023年12月22日時点
国立感染症研究所
概要
- 2022年5月以降に報告されている世界的なエムポックスの流行ではクレードIIbの エムポックスウイルス(以下、MPXVという) が原因であると報告されているが、コンゴ民主共和国では以前よりMPXV クレード Iによるエムポックスの流行が知られており、2023年は過去最大の感染者数が報告されている。また、同国内で発生した性的接触によるクレードIの流行が報告された。
- コンゴ民主共和国以外ではMPXV クレード Iの感染事例の報告はない。また、日本国内でも12月13日現在228例のエムポックス症例が探知されているが、MPXV クレード Iの感染症例は探知されていない。
- 日本国内で使用されているエムポックスのPCR検査は、MPXV クレード Iの検知が可能であり、現在研究が行われている治療薬、ワクチンについても有効性が示唆されている。ただし、特にヒトにおけるエムポックスに関する知見は主に2022年以降のMPXV クレード IIbの世界的流行において蓄積されたものであり、引き続き知見の蓄積が必要である。
- MPXV クレード Iが世界的に拡大している可能性は低いと考えられ、現時点では、国内に輸入される可能性は低く、引き続き男性間で性交渉を行う者(MSM:Men who have sex with men)の集団以外での感染リスクは低いと考えられる。一方で、MPXV クレード IはMPXV クレード IIよりも重症化するリスクが高い可能性が指摘されており、診断、治療体制の整備や疫学調査といったエムポックス対策の継続が必要である。
- 詳細
 |
国立感染症研究所インフルエンザ・呼吸器系ウイルス研究センター第一室
全国地方衛生研究所 |
- 詳細
今冬のインフルエンザについて (2022/23シーズン)
国立感染症研究所
厚生労働省健康・生活衛生局感染症対策部感染症対策課
令和5年12月19日
はじめに
今冬のインフルエンザについて、主に感染症発生動向調査に基づき、全国の医療機関、保健所、地方衛生研究所、学校等からの情報、国立感染症研究所関係部・センターからの情報をまとめました。本報告は疫学的及びウイルス学的観点から公衆衛生上有用と思われる知見をまとめたものです。比較のために、多くの場合、過去の数シーズンの情報も合わせて掲載しています。なお、2022/23シーズンは、複数の発生動向に関する指標の水準が2020/21シーズンと2021/22シーズンのそれを上回りましたが、新型コロナウイルス感染症が流行する前のシーズンと比較すると低い水準でした。また、2020年以降、世界的な流行となった新型コロナウイルス感染症そのものや、その流行に対する個人の受療行動や公衆衛生上の対応等により、インフルエンザの発生動向や関連する指標への影響が生じていた可能性があり、その解釈に注意が必要であることを申し添えます(新型コロナウイルス感染症は、感染症法上、2020年2月1日から2021年2月12日までは指定感染症、2021年2月13日から2023年5月7日までは「新型インフルエンザ等感染症」としての取り扱いでした)。
本文中に示す各シーズンの表記と期間は以下のとおりです。
- 今シーズン(2022/23シーズン):2022年第36週(2022年9月5日)から2023年第25週(2023年6月25日)まで(分析対象によっては期間が多少前後します)
- 前シーズン(2021/22シーズン):2021年第36週(2021年9月6日)から2022年第35週(2022年9月4日)まで
- 前々シーズン(2020/21シーズン):2020年第36週(2020年8月31日)から2021年第35週(2021年9月5日)まで
年齢群に分けて表示する場合には、原則的には0-4歳、5-9歳、10-14歳、15-19歳、20-29歳、30-39歳、40-49歳、50-59歳、60-69歳、70歳以上とし、小児が流行の主体であるというインフルエンザの特性から小児の年齢群のみを5歳ごと、20歳から69歳については10歳ごととしていますが、一部は、0-14歳(あるいは15歳未満等の表現)、15-59歳、60歳以上という年齢群を併記している箇所もあります。
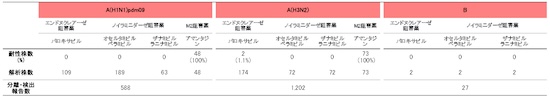
A型インフルエンザウイルスにおける同じ亜型の表記の方法に若干の違いが見られることがあります。これは、例えばヘマグルチニン(HA)の分類までを調べた情報を主とする場合(AH3亜型などと総称する)、やノイラミニダーゼ(NA)まで含めた詳しい分析を主に含む場合、などの違いによるもので、実際には同じ亜型について述べています。
例) ・A(H3N2)亜型、AH3亜型
・A(H1N1)pdm09亜型、AH1pdm09亜型、AH1pdm亜型
本記事の本文は下記のPDF版からご覧ください。
- 詳細
百日咳は、百日咳菌(Bordetella pertussis)の気道感染により、約7~10日間の潜伏期間を経てカタル症状を呈して発症する。その後長く続く咳嗽に加え、連続性の咳嗽発作や咳嗽後の嘔吐、吸気性の笛声(whoop)といった特徴的な症状を呈する。合併症として二次性の肺炎やけいれん、脳症などを発症することがあり、特にワクチン未接種の乳幼児が罹患すると重篤化し易い。新生児やワクチン未接種の乳児が発症すると咳が明確でないまま重篤な無呼吸発作などを起こし、それに伴いチアノーゼやけいれんを認めることがある。呼吸管理のため入院加療となった症例や死亡例も報告されてきた1)
2017年12月31日まで、百日咳は感染症法上の5類感染症定点把握対象疾患であった。全国約3,000の小児科定点医療機関において診断された百日咳患者の年齢(群)、性別が毎週報告され、小児における年別・性別分布、流行状況などを把握する重要な情報源として活用されてきた。しかし、小児科定点からの報告では成人症例や定点医療機関の診療圏外で発生した集団感染例を把握することが困難であった。また、届出基準として臨床診断(2週間続く咳嗽と特徴的な咳嗽)のみが定められていたため、重症例でありながら咳嗽の期間が短く届出基準を満たさない症例は報告の対象外となっていた。その他、感染源や予防接種歴などの情報が報告に含まれないなどの課題があり、百日咳の疾病負荷全体を評価する報告システムが必要であった2)。
より正確な国内の百日咳の把握の必要性が高まるなか、わが国では2018年1月1日から国内の百日咳サーベイランスはすべての医師が届出を行う5類全数把握対象疾患へと変更された。全数把握対象疾患としての届出基準は百日咳の臨床的特徴を有するもの(百日咳に特有な咳嗽、白血球数増多、肺炎、痙攣、脳症)を診察した結果百日咳を疑い、かつ検査診断により百日咳と診断した場合である。特異度の高い検査法として、遺伝子検査の1つである百日咳菌LAMP法(loop-mediated isothermal amplification)が開発され3)、同検査の健康保険適用認可などの環境も整ったことがその背景にあった。なお、前述のように、届出にあたっては原則として検査診断が求められている。2021年6月3日からは、イムノクロマト法による病原体の抗原の検出が届出基準に追加された4)。
全数把握対象疾患への変更に伴い、サーベイランスの充実を図るため、届出の手順や最適な検体の採取時期などを示したガイドラインが作成され、現在は「感染症法に基づく医師届出ガイドライン(第二版)(以下、届出ガイドラインと略す。)」5)として示されている。本稿においては、2022年1月3日から2023年1月1日まで(2022年第1週から第52週まで)に診断された百日咳のサーベイランス結果のまとめを還元することを目的とする。なお、過去のまとめについては国立感染症研究所、百日咳のウェブサイトを参照のこと(https://www.niid.go.jp/niid/ja/diseases/ha/pertussis.html)。
2022年1月3日から2023年1月1日までに感染症発生動向調査(NESID)へ499例の百日咳の報告があった(2023年1月5日現在)。全届出症例499例のうち、百日咳患者の都道府県別人口10万人あたりの報告数は、徳島県(9.4例)が最も多く、次いで福島県(2.5例)、宮崎県(1.4例)であった。
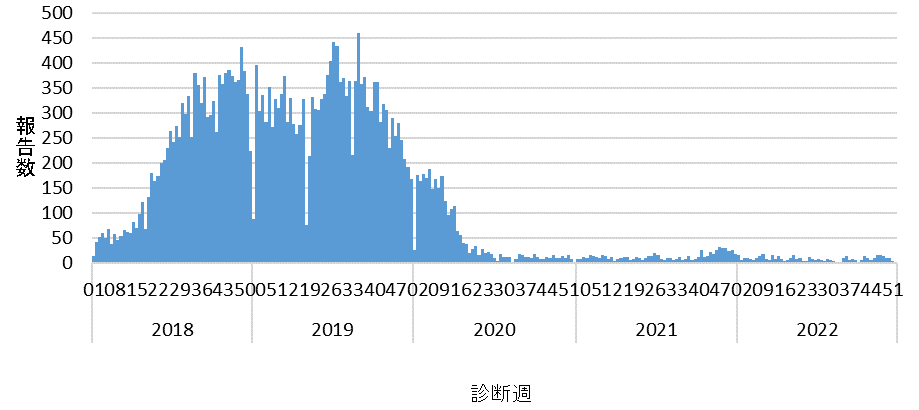
感染症法上の届出基準を満たし、かつ届出ガイドラインに合致するとみなされた患者は469例(94%)であった。以下は、特記しない限り届出ガイドラインの基準を満たした患者について述べるものである。2022年の患者報告数は2021年(712例)より減少した(図1)。
図1. 2018年~2022年診断週別百日咳報告数*
(*)百日咳 感染症法に基づく医師届出ガイドライン(第二版)に則った症例のみを抽出 https://www.niid.go.jp/niid/ja/pertussis-m/610-idsc/10875-pertussis-guideline-211228.html
図2. 百日咳症例の年齢分布と予防接種歴(2022年第1週~第52週(診断週))(n=469*)
(*)百日咳 感染症法に基づく医師届出ガイドライン(第二版)に則った症例のみを抽出
百日咳患者の年齢分布並びにワクチン接種回数を図2に示す。初回ワクチン接種前の時期を含む6か月未満児(3%)、6か月から5歳未満までの小児(25%)、5歳から15歳未満までの学童期の小児(27%)、さらには小児科定点報告では把握できていなかった20〜30代の成人(19%)においても患者が散見された。全体の42%に当たる196例に4回の百日せき含有ワクチン接種歴があり、5~15歳未満がその51%(100/196例)を占めた。
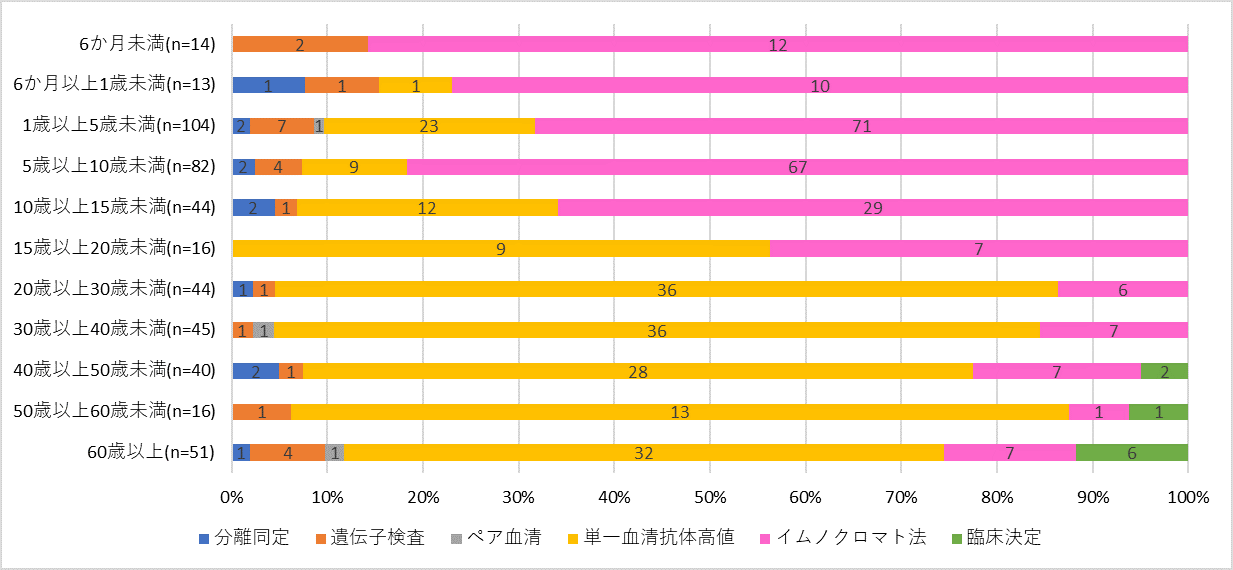
検査診断方法について複数の検査方法の記載がある場合、診断の確からしさに基づいて分離同定>遺伝子検査>ペア血清>単一血清抗体価高値>イムノクロマト法、の順に一つの診断方法を選択した(今回の更新情報でイムノクロマト法以外の診断方法を優先した理由については後述)。そのうち、全届出症例499例では、単一血清抗体価高値とイムノクロマト法がそれぞれ45%であった。血清抗体価に基づく診断では、ペア血清を用いることが望ましいが、ペア血清による有意な抗体価上昇で診断された患者は1%であった。その他、百日咳菌の分離同定2%、遺伝子検査5%、臨床診断に加えて疫学的リンクありの患者は2%であった。単一血清抗体価高値のみで診断、報告された全227例のうち、届出ガイドラインの基準を満たす検査結果(抗PT-IgG抗体100 EU/mL以上、百日咳IgM/IgA抗体のいずれか、あるいは両方陽性)に基づいた報告例は199例(88%)であった。実施された検査方法の年齢別割合をみると、15歳未満ではイムノクロマト法の実施割合が高く、15歳以上では単一血清抗体価による診断例の割合が50%以上と高かった(図3)。各種検査法については、発症日からの経過期間に基づいて推奨されるそれぞれの検査法を選択することが重要であり、詳細は届出ガイドラインを参照されたい5)。なお、国内で保険収載されている百日咳菌LAMP法は、感度・特異度が高いうえに迅速に結果を得ることができるため、百日咳の早期診断において積極的に活用することが推奨される。
図3. 年齢群別の検査診断法の割合(2022年第1週~第52週(診断週))(n=469*)
(*)百日咳 感染症法に基づく医師届出ガイドライン(第二版)に則った症例のみを抽出
全届出症例のうち、重症化のリスクが高い6か月未満児の患者は、報告対象期間に14例の報告があった。このうちワクチン未接種者が7例(50%)存在し、1回目の百日せき含有ワクチン接種前の時期に当たる3か月未満児の症例が6例(43%)含まれていた。また、6か月未満児の症例において推定される感染源は、同胞が最も多く(43%)、次いで母親(14%)であった。感染源不明の症例は半数を占めた(家族内不明7%、不明43%)(推定感染源の重複あり)。診断方法はイムノクロマト法が12例(86%)で最も多く、次いで遺伝子検査2例(14%)であった(2022年はこの年齢群に国際的に推奨されていない血清学的診断例は認めなかった)。症状・所見としては、肺炎1例 (7%)があった。入院歴の記載があった症例は、6か月未満児の症例では1例(7%)であり、生後6か月以上の症例では7例(1%)であった。6か月未満の患児の感染源の多くが兄姉であったことから、これらの年齢層、特に学童期における百日せき含有ワクチンの追加接種等の対策の必要性が示唆された。
百日咳のサーベイランスが原則として検査診断による全数報告に変更され、5年が経過した。小児科定点サーベイランスでは情報が不十分であった成人の百日咳や、診断方法、予防接種歴、さらには重症化のリスクが高い6か月未満児症例の感染源に関する情報が得られた。2022年の年齢別報告数では四種混合ワクチンを4回接種して間もない小児の患者の割合が大きくなっていた。この疫学的変化は新型コロナウイルス感染症(COVID-19)による行動変容が大きく影響していると考えられた。COVID-19対策として、「人と人の距離の確保」「マスクの着用」「手洗いなどの手指衛生」などの感染対策の実施が推進された6)ことにより、大幅に百日咳患者数が減少した一方、対策が実施しにくい年齢群の患者数の減少幅が小さかったため、相対的にこの年齢群の患者割合が増えたと考えられた。また、検査診断法におけるイムノクロマト法の割合は、2021年には全届出症例746 例中208例(28%)であったが、2022年は全届出症例499例中224例(45%)と増加した。本検査法は利便性が高い一方で、百日咳菌以外のBordetella属細菌等に交差反応を示すほか、患者検体にhuman anti-mouse antibody(HAMA)が含まれる場合にも陽性となる可能性が指摘されるなど注意が必要である7)。2023年以降は、新しい検査法の普及に加え、COVID-19の行動制限の緩和、個人判断による感染対策等により百日咳の発生動向が変化する可能性が高い。現行の全数報告の維持と詳細なデータの分析、それらの情報に基づいた予防策の提言および実施を引き続き行うことが重要である。
なお、感染症発生動向調査における届出基準、特に百日咳の届出ガイドラインにおける基準は、サーベイランスとして標準的な診断による患者報告を収集するためのものであり、臨床現場において医師が患者個々に対して行う診断とは異なることがあることに留意されたい。
関連資料
![]() 2022年第1週から第52週(*)までにNESIDに報告された百日咳患者のまとめ(2022年第52週週報データ集計時点 )
2022年第1週から第52週(*)までにNESIDに報告された百日咳患者のまとめ(2022年第52週週報データ集計時点 )
【参考文献】
1.Kilgore PE, Salim AM, Zervos MJ, Schmitt HJ. Pertussis: Microbiology, Disease, Treatment, and Prevention. Clin Microbiol Rev. 2016. 29: 449-86.
2.国立感染症研究所「百日せきワクチンファクトシート」平成29(2017)年2月10日
3.Kamachi K, Toyoizumi-Ajisaka H, Toda K, Soeung SC, Sarath S, Nareth Y, Horiuchi Y, Kojima K, Takahashi M, Arakawa Y. Development and evaluation of a loop-mediated isothermal amplification method for rapid diagnosis of Bordetella pertussis infection. J Clin Microbiol. 2006. 44:1899-902.
4.厚生労働省健康局結核感染症課長「感染症の予防及び感染症の患者に対する医療に関する法律第12条第1項及び第14条第2項に基づく届出の基準等について」の一部改正について 令和3年6月3日
https://www.mhlw.go.jp/content/10900000/000788097.pdf
5.百日咳 感染症法に基づく医師届出ガイドライン(第二版)
https://www.niid.go.jp/niid/ja/pertussis-m/610-idsc/10875-pertussis-guideline-211228.html
6.新型コロナウイルス感染症対策の基本的対処方針令和2年3月 28 日(令和2年5月 14 日変更)新型コロナウイルス感染症対策本部決定
https://www.kantei.go.jp/jp/singi/novel_coronavirus/th_siryou/kihon_h_0514.pdf
7.Kenji Okada, Yuho Horikoshi, Naoko Nishimura, Shigeki Ishii, Hiroko Nogami, Chikako Motomura, Isao Miyairi, Naoki Tsumura, Toshihiko Mori, Kenta Ito, Shinichi Honma, Kensuke Nagai, Hiroshi Tanaka, Toru Hayakawa, Chiharu Abe, Kazunobu Ouchi Clinical evaluation of a new rapid immunochromatographic test for detection of Bordetella pertussis antigen Sci Rep. 2022; 12
- 詳細
国立感染症研究所 実地疫学研究センター
感染症疫学センター
2023年2月3日現在
(掲載日:2023年12月14日)
カルバペネム耐性腸内細菌目細菌(CRE)感染症*は、2014年9月19日より感染症法に基づく5類全数把握対象疾患となった。届出対象はCREによる感染症を発症した患者であり、保菌者は対象外である(届出基準、届出票についてはhttps://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou11/01-05-140912-1.html参照)。なお、感染症法に基づく届出の基準として示されたCREの判定基準値は病院で用いられている判定基準値と異なることがある(文末参考)。
2023年2月3日現在、2021年第1週~第52週(2021年1月4日~2022年1月2日)にCRE感染症と診断され、報告された症例は2,066例であり(図1)、うち届出時点の死亡例は49例(2%)であった。報告数は、2019年は2,333例と過去最多であったが、2020年は1,956例へ減少し、2021年は2,066例であった。
男性が1,292例(63%)、診断時の年齢中央値は77歳(四分位範囲 68-85)、70歳以上の症例は1,493例(72%)であった。診断名†は、尿路感染症 696例(34%)、菌血症・敗血症 519例(25%)、肺炎406例(20%)の順に多かった(表1)。菌が分離された検体は、尿613例(30%)、血液579例(28%)、喀痰 368例(18%)の順に多かった(表2)。2019年から2021年の3年間において、診断名および菌が分離された検体の内訳は同様の傾向であった。分離された菌種は、Klebsiella aerogenes 800例(39%)、Enterobacter cloacae 514例(25%)、Klebsiella pneumoniae 215例(10%)、Escherichia coli 128例(6%)の順に多く報告された(表3)。これらの4菌種が多く報告される傾向は、2019年から2021年の3年間で同様であった。薬剤耐性の確認に用いた薬剤名の記載があったのは1,992例(96%)で、メロペネムの基準のみが432例 (22%)、イミペネムかつセフメタゾールが1,037例 (52%)、両方が記載されていたものが523例(26%)だった。2021年は、全ての都道府県から報告があり、東京都 (208例)、大阪府(186例)、愛知県(160例)の順に多く報告されていた。
* 感染症の予防及び感染症の患者に対する医療に関する法律等の一部を改正する法律の施行に伴う厚生労働省関係省令の整備等に関する省令(令和5年厚生労働省令第79号)により、カルバペネム耐性腸内細菌科細菌感染症からカルバペネム耐性腸内細菌目細菌感染症へ名称変更 (https://www.mhlw.go.jp/content/10900000/001101196.pdf)
† 診断名は症状として報告された情報を用い集計した
- 詳細
鳥インフルエンザA(H7N9)ウイルスによる感染事例に関するリスクアセスメントと対応
2022年4月22日現在
2023年12月8日一部更新
国立感染症研究所
PDF
更新点
2023年12月8日 「日本人渡航者が感染するリスク」内に受診時に鳥類との接触歴を伝える必要性について追記
目次
- 背景
- 疫学的所見
1)事例の概要
2)臨床情報
3)感染源・感染経路 - ウイルス学的所見
- 日本国内の対応
- リスクアセスメントと今後の対応
背景
A型インフルエンザウイルス(H7N9亜型)(以下、H7N9ウイルス)は、家きんや野鳥で流行していた少なくとも3種類の異なるA型インフルエンザウイルスの遺伝子再集合体であると考えられ (Liu WJ, 2021)、ヒトに感染すると重篤な症状を来し得ることが報告されている(CDC, 2017)。中国における2018-2019年シーズン以降のH7N9ウイルスの感染者数は1例のみであった。2018-2019年シーズン以降の状況について疫学情報及びリスクアセスメントを更新する。