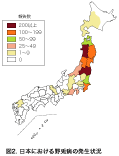
野兎病(tularemia)は野兎病菌(Francisella tularensis )による急性熱性疾患で、代表的な動物由来感染症の一つである。自然界において本菌はマダニ類などの吸血性節足動物を介して、主にノウサギや齧歯類などの 野生動物の間で維持されており、これらの感染動物から直接あるいは間接的にヒトが感染する。近年、わが国において野兎病は非常に稀な感染症であるが、本菌 は今日でも国内の野生動物間で維持されていると考えられること、また、ヒトが海外の発生地で感染したり、本菌が生物テロに使用される可能性のある病原体と してリストアップされるなど、留意すべき感染症の一つである。
疫 学
| 発生状況:野兎病は北米、北アジアからヨーロッパに至る、ほぼ北緯30度以北の北半球に広く発生している(図1)。米国やスウェーデンなどの海外の汚染地域では毎年散発的に起っており、ときに流行を示すこともある。 | 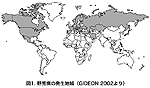 |
| 図1. 野兎病の発生地域(GIDEON 2002より) |
戦後の患者数の急増は、食糧難のためにノウサギを捕獲・解体する機会が増加し、また1964年以降は経済の高度成長に伴い生活様式が変化し、ノウサギとの接触機会が減少したためと考えられている。
感染源動物:野兎病菌の自然保有例は世界的に哺乳類の190種、鳥類23種、両棲類3種、マダニなどの無脊椎動物88種で報告 されている。日本におけるヒトへの感染の90%以上は、ノウサギとの接触によるものである。他に感染源や菌が分離された動物としてネコ、リス、ツキノワグ マ、ヒミズ、ヤマドリ、カラス、キジ、一部のマダニ類などがある。
感染様式:大部分の患者は保菌動物の剥皮作業や肉の調理の際に、菌を含んだ血液や臓器に直接触れることにより感染している。さ らに、マダニ類やアブ類等の吸血性節足動物による刺咬からの感染例も報告されている。ペットに付着したマダニ除去の際に、虫体を潰して体液が目に飛び込ん だり、指が汚染されることによるものもある。海外では感染動物との直接接触や吸血性節足動物の刺咬以外に、保菌野生齧歯類の排泄物や死体によって汚染され た飲用水 や食物による経口感染、また、死骸が紛れ込んだ干し草等の粉塵の吸入による呼吸器感染も報告されている。ヒトからヒトへの感染はないとされているが、患者 の潰瘍部からの浸出物などもヒトへの感染源となりうるので、注意が必要である。
病原体
野兎病菌はグラム陰性の小短桿菌 (0.2×0.3~0.7μm)で、多形性を示す。好気性菌で、宿主のマクロファージ内で増殖する細胞内寄生細菌である。野兎病菌は水や泥、死体中などで 数週間は生存可能とされているが、熱に対しては弱く、55℃10分程度で容易に死滅する。
| 現在まで、特定の病原性因子は解明されていない。血清型は1種で、菌株の生化学的性状および病原性などから、本菌種は3亜種に分類されるが(表1)、1)、2)がほとんどの野兎病の起因亜種である。 |  |
| 表1. Francisella 属の種、亜種、biovarの性状と分布 |
1)subsp. tularensis は主に北米に分布し、10個以下の菌で感染が成立する強毒型である。有効な抗菌薬での治療がなされない場合、致死率は5%である。Type Aあるいはsubsp. nearctica と呼ばれていた。
2)subsp. holarctica はユーラシア大陸から北米にかけて広い範囲に分布し、日本に分布する野兎病菌もこの亜種である。病原性は弱く、この亜種の感染による死亡例は極めて稀である。Type Bあるいはsubsp. palaearctica と呼ばれていた。
3)subsp. mediasiatica は中央アジアから旧ソ連の一部地域に分布し、病原性は強くない。
さらに北米に分布する別種Francisella novicida を、その遺伝子配列の相同性から亜種とするよう提唱されている。抗原性により上記3亜種とは区別できる。
臨床症状
| 野兎病はペストに類似した臨床症状を呈するが、感 染初期においては特徴がなく、しばしば誤った診断がつけられる。野兎病は急性熱性疾患で、感染後3日目をピークとした1週間以内(稀に2週間~1カ月)の 潜伏期間後に、突然の発熱(38~40℃)、悪寒・戦慄、頭痛、筋肉痛、関節痛などの感冒様の全身症状が認められる。 |  |
| 表2. 野兎病の臨床病型 |
その後弛緩熱となり、長く続く。野兎病菌の感染力は極めて強く、目などの粘膜部分や皮膚の細かい傷はもとより、健康な皮膚からも 侵入できるのが特徴である。皮膚から侵入した野兎病菌はその部位で増殖し、侵入部位に関連した所属リンパ節の腫脹、膿瘍化、潰瘍または疼痛を引き起こす。 病原菌の侵入部位によって様々な臨床的病型を示す(表2)。我が国では90%以上がリンパ節腫脹を伴う例で、60%がリンパ節型、20%が潰瘍リンパ節型である。一方、米国では潰瘍リンパ節型が多い。また、各病型の経過中、3週目頃に一過性に蕁麻疹様、多形浸出性紅斑などの多様な皮疹(野兎病疹)が現れることがある。
鑑別すべき類似疾患として、ツツガムシ病、日本紅斑熱、結核、ネコ引っ掻き病、ペスト、ブルセラ症などがある。
病原診断
診断には患者の臨床症状、汚染地域への立ち入り、野外での活動状況、動物や動物死骸との接触歴などの問診が重要である。最も確実な検査は患者からの病原体の分離・同定であるが、その他にゲノムDNAや菌体抗原の検出、および血清中の特異抗体検出などが実施される。
病原体検査:通常病原体の分離培養は、腫脹したリンパ節の膿汁を野兎病菌用培地に直接接種する方法と、マウス腹腔内に接種した 後、発症または死亡後の血液、脾臓、肝臓を培地に接種する方法がある。本菌は通常検査室で用いられる培地ではほとんど増殖せず、適当な培地を用いても数日 を要し、困難な場合も多い。野兎病菌はシステイン要求性であり、8%ヒツジ脱繊血加ユーゴン寒天培地などが用いられている。雑菌の混入がある場合には、ペ ニシリン、ポリミキシンB、シクロヘキサミドなどを培地に添加する。患部や組織のスタンプ標本での直接あるいは間接蛍光抗体法などの免疫学的方法による、 菌体抗原の検出も有用である。
近年、野兎病菌の16SリボソームRNA遺伝子、外膜蛋白質遺伝子(fopA)や17 kDaリポ蛋白質遺伝子(tul4)などを対象としたPCR法や、リアルタイムPCR法などの高感度なゲノムDNA検出法が開発され、検体からの直接検出 や菌の同定に有効である。また、野兎病菌ゲノムの繰返し塩基配列領域などの解析で、分離株の型別ができるようになってきている。
血清学的検査:野兎病菌に対する血中抗体価は発病2週目頃から上昇し、4~6週目に最高値を示し、その後も長期間維持される。 ホルマリン不活化菌体を抗原とした試験管凝集反応で、ペア血清で4倍以上の抗体価の上昇、あるいは単一血清で40倍以上を陽性とする。高感度で、使用する 血清や抗原が少量ですむ微量凝集反応法(マイクロプレート法)も行われている。凝集反応ではブルセラ属菌との交差反応があるので、注意を要する。他の血清 学的診断法としてELISA法、ウエスタンブロット法などが行われる。野兎病検査のためのキットや試薬等は、国内では販売されていない。
治療・予防
野兎病では抗菌薬を用いた治療が有効で、早期の治療開始が重要である。
全身治療:硫酸ストレプトマイシン1 g/日(またはゲンタマイシン40~60 mg/日)の筋注と同時に、テトラサイクリン1 g/日・分4(またはミノサイクリン200 mg/日・分2)の経口投与を2週間続ける。症状が残れば、テトラサイクリン系抗菌薬を半量にした内服をさらに1~2カ月間続ける。ペニシリン系、セファ ロスポリン系抗菌薬は無効である。
局所治療:膿瘍化したリンパ節に対しては、太めの注射針で3~4日ごとに穿刺排膿する。症例によってはストレプトマイシン 0.1~0.2 gを1 mlの生理食塩水に溶解し、注入する。多くは2~3回で膿瘍は消退する。切開排膿は難治性瘻孔を作りやすいので、病巣の完全な掻爬が必要である。
予防:流行地においては死体を含め、野生ノウサギや齧歯類などとの接触は避け、またダニや昆虫の刺咬を防ぐこと(衣服、忌避剤 など)、生水の飲用をしないなどの注意も必要である。検査室で野兎病を疑う検体を取り扱う際には、手袋等での防護が必要である。なお野兎病菌の培養は、バ イオセイフティ・レベル3での取り扱いが必要である。旧ソ連では弱毒生ワクチン(RV株)が広く用いられた。米国では実験室のバイオハザード対策として、 一部で弱毒生ワクチン(LVS株)が使用されているが、日本にはない。
感染症法における取り扱い(2012年7月更新)
全数報告対象(4類感染症)であり、診断した医師は直ちに最寄りの保健所に届け出なければならない。
届出基準はこちら
【参考文献】
1)大原義朗:野兎病.動物由来感染症その診断と対策、pp209-213、神山恒夫、山田章雄編、真興交易、東京、2003.
2)藤田博己:野兎病.モダンメディア.50: 99-103, 2004.
3)Morner T & Addison E(2001): Tularemia In Infectious Diseases of Wild Mammals. (Williams E. S. & Barker I. K. eds.), 303-312, Iowa State University Press.
4)Ellis J, Oyston PCF, Green M, et al: Tularemia. Clin. Microbiol. Rev. 15:631-646, 2002.
5)Petersen JM & Schriefer ME:Tularemia:emergence/re-emergence. Vet. Res. 36: 455-467, 2005
(国立感染症研究所獣医科学部 藤田 修 堀田明豊 棚林 清)