令和5年5月26日改訂
国立感染症研究所
エムポックスは、モンキーポックスウイルス(別名 エムポックスウイルス、以後エムポックスウイルスと表記)感染による急性発疹性疾患である。感染症法では4類感染症に位置付けられている。主にアフリカ中央部から西部にかけて発生しており、自然宿主はアフリカに生息するげっ歯類が疑われているが、現時点では不明である。稀に流行地外でも、流行地からの渡航者等に発生した事例がある。症状は発熱と発疹を主体とし、多くは2−4週間で自然に回復するが、小児等で重症化、死亡した症例の報告もある。
病原体
ポックスウイルス科は、感染細胞の細胞質で増殖する、遺伝物質として二本鎖DNAを持つ巨大なエンベロープウイルスで、脊椎動物に感染するChordopoxvirus亜科と、節足動物に感染する Entomopoxvirus 亜科に分類される。Chordopoxvirus 亜科はOrthopoxvirus(オルソポックスウイルス)、 Parapoxvirus、 Capripoxvirus、 Sulpoxvirus、 Leporipoxvirus、 Avipoxvirus、 Yatapoxvirus、Molluscipoxvirus の8属と、未分類のウイルスからなる。
オルソポックスウイルス属のウイルスの形態はレンガ状で、その長径は300nmを超える巨大なウイルスである(写真1)。感染性ウイルス粒子は、細胞内で形成される細胞内成熟ウイルスと、細胞内成熟ウイルスが感染細胞膜から出芽し、細胞膜由来脂質膜をさらに被った細胞外外皮ウイルスからなる。両者の脂質膜上のウイルス糖タンパクは異なる。個体間の感染には細胞内成熟ウイルスが関与し、感染個体内での感染の拡大には主に、細胞外外皮ウイルスが関与すると考えられている。
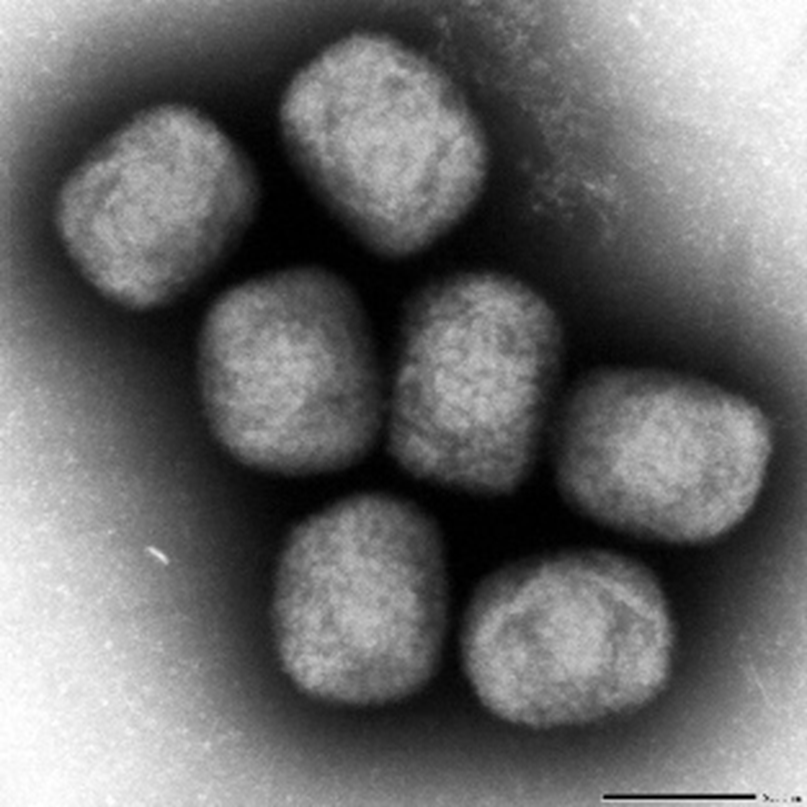
写真1. エムポックスウイルスの電子顕微鏡写真
(形態的にはエムポックスウイルス、天然痘ウイルス、ワクチニアウイルス等を相互に区別できない)
オルソポックスウイルス属には、エムポックスウイルス、痘そうウイルス(天然痘ウイルス)、ワクチニアウイルス(種痘に用いられるウイルス)、牛痘ウイルス等が含まれる。
エムポックスウイルスには大きく分けてコンゴ盆地系統群(クレード)と西アフリカ系統群(クレード)の2種類の遺伝的系統群があり、コンゴ盆地系統群は西アフリカ系統群に比較して、重症化しやすく、またヒトからヒトへの感染性が高いとされる。
感染源・感染経路
エムポックスウイルスの動物からヒトへの感染経路は、感染動物に咬まれること、あるいは感染動物の血液・体液・皮膚病変(発疹部位)との接触による感染が確認されている。自然界ではげっ歯類が宿主と考えられているが、自然界におけるサイクルは現時点では不明である。
ヒトからヒトへの感染は稀であるが、濃厚接触者の感染や、リネン類を介した医療従事者の感染の報告があり(Aaron TF. 2005, Aisling V. 2020)、患者の飛沫・体液・皮膚病変(発疹部位)を介した飛沫感染や接触感染があると考えられている。
流行地
エムポックスは1970年にザイール(現在のコンゴ民主共和国)で初めて報告されて以降、アフリカ中央部から西部にかけて主に発生してきた。
2022年4月24日現在、アフリカ大陸では中央アフリカ共和国、コンゴ民主共和国、ナイジェリアで発生が持続しており、特にコンゴ民主共和国では2022年1月以降1,152例の患者と55例の死亡例が報告されている(WHO AFRO, 2022)。
一方、アフリカ以外でも、過去に流行地域からの帰国者で散発的に発生報告が見られていた。2018年の英国からの報告では、ナイジェリアからの帰国者2例と、患者に対応した医療従事者1例が報告され、患者の使用したリネン類からの感染が疑われている(UK HSA, 2022)。アフリカ以外での最大の発生は、2003年4月に米国テキサス州でガーナから輸入されたエムポックスに感染したげっ歯類を原因とする事例である。これらのげっ歯類の輸入動物は動物販売業者でプレーリードッグと接し、その後ペットとして販売されたプレーリードッグを介して47例のヒト症例が報告された。本事例において死亡例は報告されず、またヒトヒト感染の報告もなかった(CDC, 2021)。また、本事例に関連してテキサス州に輸入されたげっ歯類のうち、アフリカヤマネ17匹が2003年5月8日に日本へ輸入されたことが判明したが、これらのアフリカヤマネは全頭が死亡もしくはエムポックスウイルス検査陰性が確認され、国内での発生にはつながらなかった。
日本国内では感染症発生動向調査において、集計の開始された2003年以降、輸入例を含めエムポックス患者の報告はない。
2022年5月、海外渡航歴のないエムポックス患者が英国より報告され、また、欧州、米国でも患者の報告が相次いでおり、調査が進められている。
臨床像
エムポックスの潜伏期間は5~21日(通常6~13日)とされる(CDC, 2021)。潜伏期間の後、発熱、頭痛、リンパ節腫脹、筋肉痛などが1~5日続き、その後発疹が出現する。発疹は典型的には顔面から始まり、体幹部へと広がる。初期は平坦であるが、水疱、膿疱化し痂皮化した後、発症から2~4週間で治癒する(写真2)。発疹は皮膚だけではなく、口腔、陰部の粘膜、結膜や角膜にも生じることがあるが、特に初期においては水痘や麻しん、梅毒などのその他の発疹症との鑑別が困難なことがある。リンパ節腫脹を呈する頻度が高く、類似した皮膚病変を示す天然痘との鑑別に有用とされる(Andrea M. 2014)。
致命率は0~11%と報告され(Skelenovska N, 2018)、特に小児において高い傾向にある(Jezek Z, 1987)。ただし、先進国では死亡例は報告されていない。
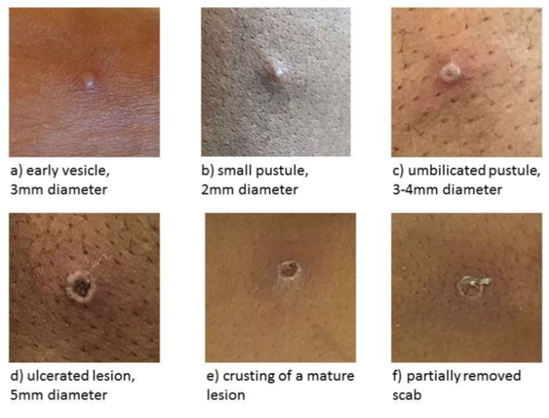
写真2. エムポックスでみられる皮疹(UK HSA. 2022)
診断においては、皮膚病変が類似する水痘、そしてエムポックス以外のオルソポックスウイルス感染症である天然痘(自然界には存在しない)、牛痘(主に欧州から中央アジアに存在)、そして野生に分布するワクチニアウイルス感染症(インド、南アメリカに存在)との鑑別が重要である。
水疱擦過物の塗沫(Tzanck smear)、水疱内容物、痂皮、血液が検査材料となりうる。電子顕微鏡によるウイルス粒子の確認、蛍光抗体法によるウイルス抗原の検出、抗ウイルス抗体の検出等が可能であるが、オルソポックスウイルス属の他のウイルスとの判別は不可能である。
そこでエムポックスの特異的診断法は上記の水疱内容物や痂皮などを検体として用いた遺伝子検査やウイルス分離による。遺伝子検査はエムポックスウイルス遺伝子に特異的なPCRによる診断を行う。エムポックスが疑われた場合は、最寄りの保健所を経由して国立感染症研究所での検査を実施する。
治療法
対症療法が行われる。一部の抗ウイルス薬について、in vitroおよび動物実験での活性が証明されており、エムポックスの治療に利用できる可能性がある。
シドフォビルはサイトメガロウイルスの治療などに海外で使用されている抗ウイルス薬であり、動物実験でエムポックスへの有効性が確認されている。シドフォビルの誘導体であるBrincidofovir(CMX001)も同様に動物実験での有効性が確認されており、シドフォビルと比較し有害事象が少ないとの報告もあるが、国内では現在流通していない。
Tecovirimat(ST-246)も動物実験でオルソポックスウイルス感染症に有効であることが示され、またヒトに対しての安全性も確認されている。米国では天然痘に対する承認が得られており、エムポックスに対してはInvestigational New Drug (IND)としての使用が可能である。欧州で天然痘、エムポックスに対しての承認が得られている。国内ではBrincidofovir同様現在流通していない。
予防法
1)家庭、市中における感染対策について
発熱、皮疹がありエムポックスが疑われる場合、マスク着用を行い、咳エチケットを守り、手指衛生を行う。また、患者が使用したリネン類から感染した報告があることから、使用したリネン類や衣類は手袋などを着用して直接的な接触を避け、密閉できる袋に入れて洗濯などを行い、その後手洗いを行う。
2)病院における確定症例、疑い症例への感染対策について
確定患者および疑い患者に対しては飛沫予防策、接触予防策を取る必要がある。
エムポックスの主な感染経路は接触感染や飛沫感染であるが、水痘、麻疹等の空気感染を起こす感染症が鑑別診断に入ること、エムポックスに関する知見は限定的であること、他の入院中の免疫不全者における重症化リスク等を考慮し、現時点では、医療機関内では空気予防策を実施することが推奨される。
また、診療行為に伴うエアロゾル感染の可能性が否定できないため、N95マスクなど空気予防策を取る事を検討する。
3)ワクチンについて
天然痘のワクチンである痘そうワクチンがエムポックス予防にも有効であるが、日本では1976年以降、痘そうワクチンの接種は行われていない。エムポックスウイルス曝露後4日以内に痘そうワクチンを接種すると感染予防効果が、曝露後4-14日で接種した場合は重症化予防効果があるとされている(CDC. 2021)。
感染症法における取り扱い
感染症法において4類感染症に指定されており、診断した医師は直ちに最寄りの保健所に届出が必要である。
届出基準、届出様式は厚生労働省ホームページを参照のこと。
参考文献
- Aaron T F, et al.. Evaluation of human-to-human transmission of monkeypox from infected patients to health care workers. Clin Infect Dis. 2005 Mar 1;40(5):689-94.
- Aisling V, et al.. Human-to-Human Transmission of Monkeypox Virus, United Kingdom, October 2018. Emerg Infect Dis. 2020 Apr;26(4):782-785.
- Andrea M. et al.. Human Monkeypox. Clin Infect Dis 2014 Jan; 58(2): 260-7
- CDC. Monkeypox, 17 Nov. 2021,
https://www.cdc.gov/poxvirus/monkeypox/index.html - ECDC. Factsheet for health professionals on monkeypox, 10 Dec. 2019
https://www.ecdc.europa.eu/en/all-topics-z/monkeypox/factsheet-health-professionals - Jezek Z, et al.. Human monkeypox: clinical features of 282 patients. J Infect Dis. (1987) 156:293–8. 10.1093/infdis/156.2.293
- Saijo M, et al.. 2008. “Diagnosis and Assessment of Monkeypox Virus (MPXV) Infection by Quantitative PCR Assay: Differentiation of Congo Basin and West African MPXV Strains.” Japanese Journal of Infectious Diseases 61 (2): 140–42.
- Sklenovska. N, et al.. Emergence of Monkeypox as the Most Important Orthopoxvirus Infection in Humans. Front Public Health. 2018 Sep 4; 6:241
- UK HSA. Guidance Monkeypox, 2022
https://www.gov.uk/guidance/monkeypox - WHO. Monkeypox, 9 Dec. 2019
https://www.who.int/news-room/fact-sheets/detail/monkeypox - WHO AFRO. Weekly Bulletin on Outbreaks and Other Emergency Week 19: 2-8 May 2022
https://apps.who.int/iris/bitstream/handle/10665/354215/OEW19-0202052022.pdf - 厚生労働省. 感染症法に基づく医師の届出のお願い エムポックス
https://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou11/01-04-13.html
更新履歴
感染症の話<サル痘> IDWR 2006年14号
https://idsc.niid.go.jp/idwr/kanja/idwr/idwr2006/idwr2006-14.pdf
サル痘とは(令和4年5月20日改訂)
https://www.niid.go.jp/niid/ja/kansennohanashi/408-monkeypox-intro.html