2022年8月17日
端 緒
新型コロナウイルス感染症(COVID-19)に対するワクチンの開発は未曾有のスピードで進み、ファイザー社製およびモデルナ社製のmRNAワクチンは大規模なランダム化比較試験で高い有効性(vaccine efficacy)が示された1-3。免疫の減衰や免疫逃避能を有する変異株の出現が確認される中で、国内においても、国立感染症研究所にて、複数の医療機関の協力のもとで、発熱外来等で新型コロナウイルスの検査を受ける者を対象として、症例対照研究(test-negative design)を実施し4-5、実社会における有効性(vaccine effectiveness;発症予防効果)を検討している。これまでの暫定報告においては、B.1.1.7系統(アルファ株)およびB.1.617.2系統(デルタ株)に対して、高い有効性を示すことが確認された4-5。さらに、オミクロン株の亜系統であるBA.1/BA.2流行期においては2回接種で中程度の有効性を示す一方、3回目(ブースター)接種により、高いレベルに有効性が回復することが示された6-7。2022年6月末以降、国内におけるCOVID-19症例は急増しており、これは新たなオミクロン株の亜系統であるBA.5の流行によるものである。そこで今回は、関東地方において、BA.5が75%以上を占めるとされた7月4日から7月31日の調査における暫定結果を報告する8-9。参考として、前回報告以降のデータを含めたBA.1/BA.2が75%以上を占めるとされた1月1日から6月19日の結果についても有効率の推定を併記した。
方 法
2022年7月4日から7月31日までに関東地方の複数医療機関の発熱外来等を受診した者を対象に、検査前に基本属性、新型コロナワクチン接種歴などを含む問診票に記載いただいた。意識障害のある者、直ちに治療が必要な者、日本語での問診票に回答できない者には問診票の配布を行わなかった。のちに各医療機関で新型コロナウイルス感染症の診断目的に実施している核酸検査(PCR)の検査結果が判明した際に検査陽性者を症例群(ケース)、検査陰性者を対照群(コントロール)と分類した。発症から14日以内で、37.5℃以上の発熱、全身倦怠感、寒気、関節痛、頭痛、鼻汁、咳嗽、咽頭痛、呼吸困難感、嘔気・下痢・腹痛、嗅覚味覚障害のいずれか1症状のある者に限定して解析を行うこととした。また、期間中にすでに受診した記録のある者は本解析においては除外した。なお、2022年7月以降、一部の医療機関では、16-19歳の者も対象に含めることとしている。
ワクチン接種歴については、(1)未接種、(2)1回接種または2回接種から13日以内、(3)2回接種から14日-3ヶ月(14-90日)、(4)2回接種から3-5ヶ月(91-150日)、(5)2回接種から5ヶ月以降(151日以降)、(6)3回(ブースター)接種から13日以内、(7)3回接種から14日-3ヶ月(14-90日)、(8)3回接種から3ヶ月以上(91日以降)の8つのカテゴリーに分けた。4回接種後の者は数が非常に少ないため、今回の報告では除外して解析した。ロジスティック回帰モデルを用いて、オッズ比と95%信頼区間(CI)を算出した。多変量解析における調整変数としては、先行研究等を参照し、年代、性別、基礎疾患の有無、職業(医療従事者かそれ以外)、医療機関、カレンダー週、濃厚接触歴の有無、過去1ヶ月の新型コロナウイルス検査の有無、3ヶ月以上前の新型コロナウイルス感染症診断歴、マスクの着用状況、飲酒を伴う夕方・夜の会食への参加をモデルに組み込んだ。ワクチン有効率は(1-調整オッズ比)×100%で推定した。さらに、国民の多くが2回接種を完了している中で、2回接種と比較した3回接種の有効性を検討するため、本報告においては、調整オッズ比を元に2回接種と比較した3回接種の相対的な有効率も算出した(3回接種の対象となり得る者に限定するために、2回接種から5ヶ月以上経過した者に限定して解析を行った)。解析に際して、ワクチンの種類は区別せず、ワクチン接種歴等について、欠損値のある者は本解析では除外した。
本調査は国立感染症研究所および協力医療機関において、ヒトを対象とする医学研究倫理審査で承認され、実施された(国立感染症研究所における審査の受付番号1332、1392)。
結 果
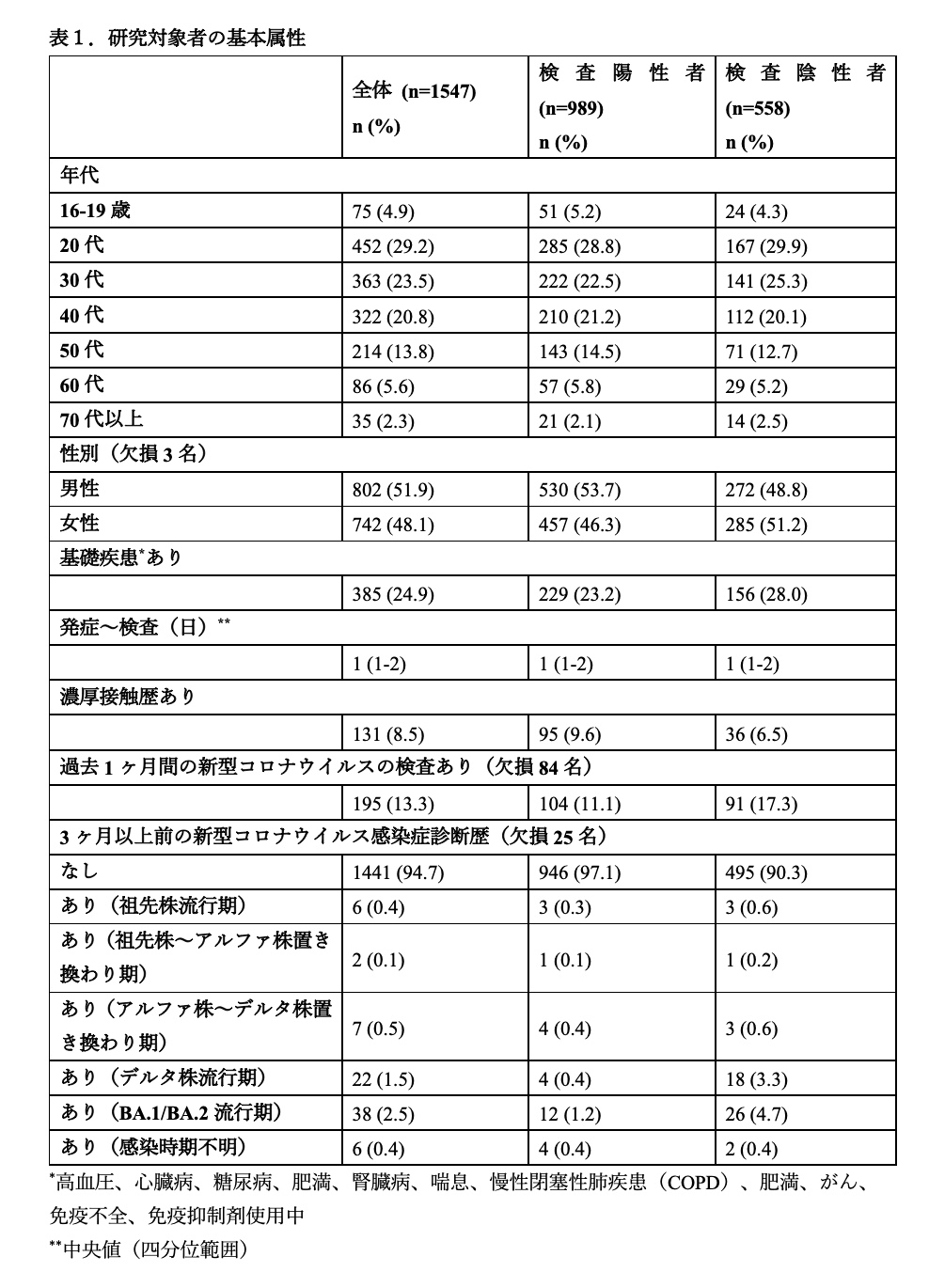
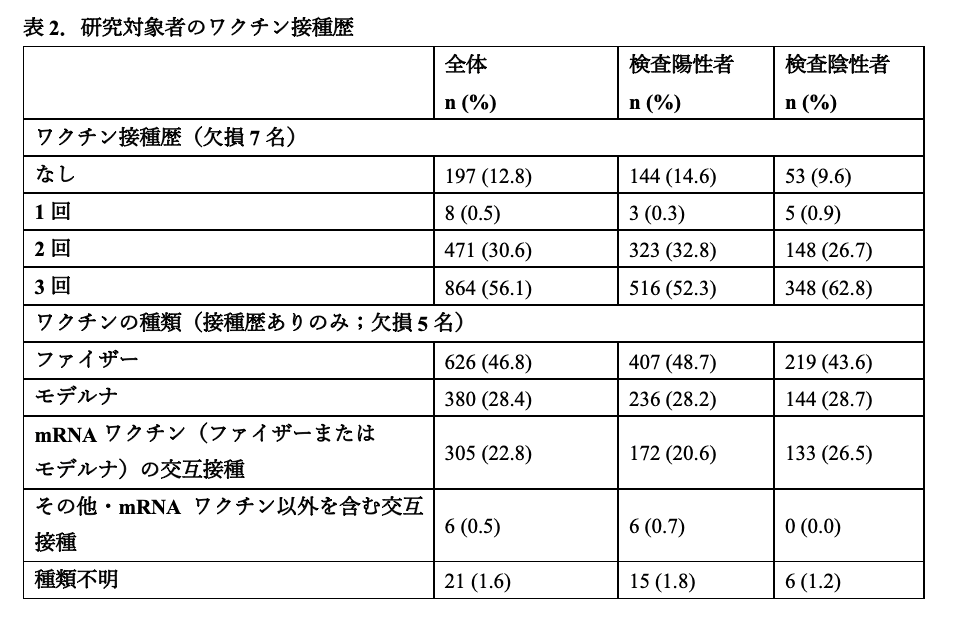
関東地方の7医療機関において、2022年7月4日から7月31日までに発熱外来等を受診した者で解析可能であった1624名が組み入れられ、うち、発症日不明および発症から15日以降に受診した者51名および4回接種後の26名を除外して解析した。解析に含まれた1547名(うち陽性989名(63.9%))においては、年齢中央値(範囲)36(16-93)歳、男性802名(51.9%)、女性742名(48.1%)であり、何らかの基礎疾患を385名(24.9%)で有していた(表1)。また、ワクチン接種歴について、未接種者は197名(12.8%)、1回接種した者は8名(0.5%)、2回接種した者は471名(30.6%)、3回接種した者は864名(56.1%)であった(ワクチン接種回数の欠損7名を除く)(表2)。
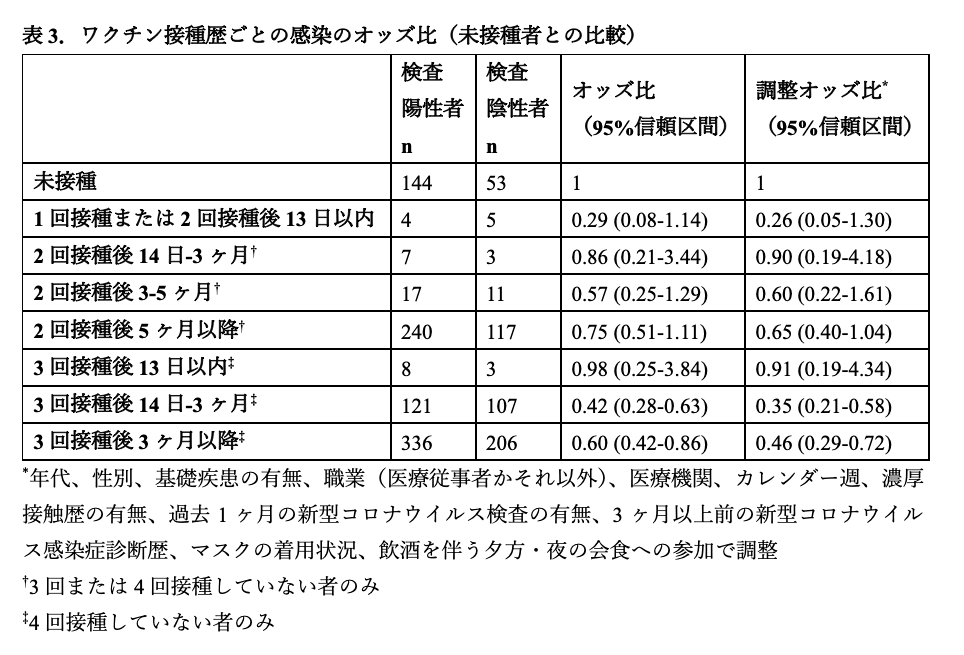
ワクチン接種歴を接種回数および接種後の期間別で8つのカテゴリーに分け、検査陽性者(症例群)と検査陰性者(対照群)とで比較した。未接種者を参照項とする調整オッズ比は、2回接種後5ヶ月以降で0.65 (95%信頼区間[95%CI] 0.40-1.04)、3回接種後14日-3ヶ月で0.35 (95%CI 0.21-0.58)、3回接種後3ヶ月以降で0.46 (95%CI 0.29-0.72)であった(表3)。
調整オッズ比を元にワクチン有効率を算出したところ、2回接種後5ヶ月以降では35% (95%CI -4-60)、3回接種14日-3ヶ月では65% (95%CI 42-79)、3回接種後3ヶ月以降では54% (95%CI 28-71)であった(図)。
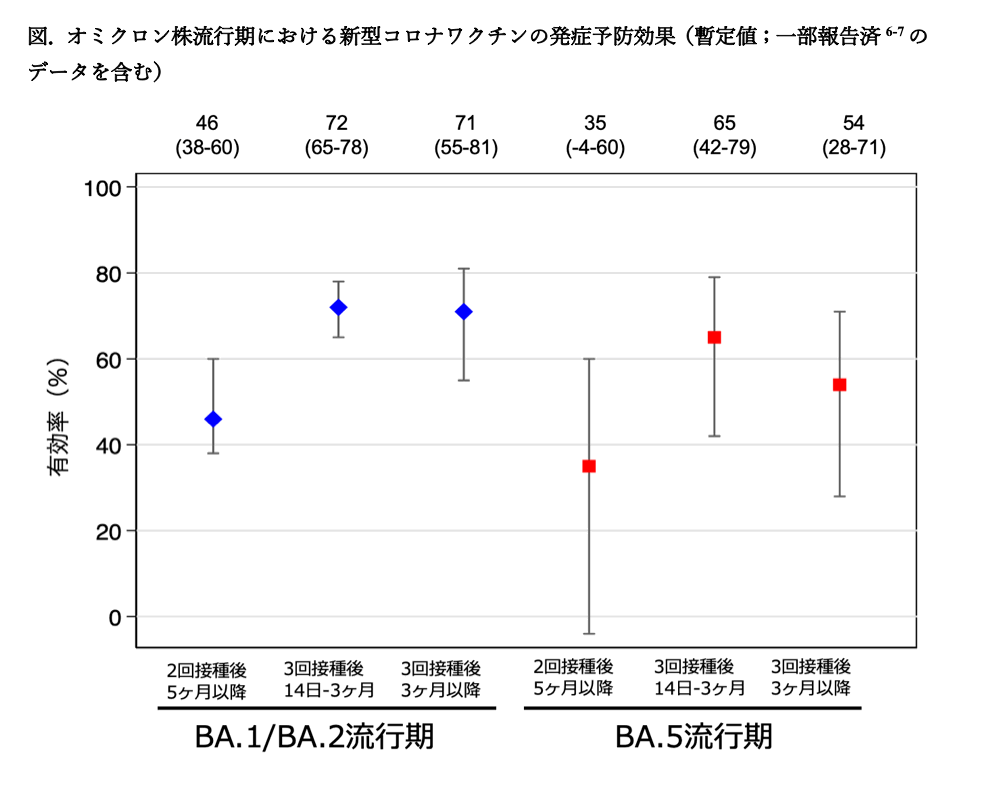
なお、参考として、1月1日から6月19日のBA.1/BA.2流行期については、解析に含まれたのは6349名(うち陽性2749名(43.3%))であり、年齢中央値(範囲)35(20-74)歳であった。この解析においては、2回接種後3-5ヶ月では50% (95%CI 30-64)、2回接種後5ヶ月以降では46% (95%CI 38-60)、3回接種14日-3ヶ月では72% (95%CI 65-78)、3回接種後3ヶ月以降では71% (95%CI 55-81)であった(図)。調整オッズ比を元に2回接種と比較した3回接種の相対的なワクチン有効率を算出したところ、3回接種14日-3ヶ月では49% (95%CI 38-58)、3回接種後3ヶ月以降では46% (95%CI 20-64)であった。
考 察
本報告では2022年7月のBA.5流行期におけるワクチンの有効性を検討した。BA.5流行期においては、2回接種後5ヶ月後には発症予防効果は低程度であった。一方で、3回(ブースター)接種により発症予防効果が中〜高程度まで高まる可能性が示された。2回接種と比較した3回接種の相対的な有効率についても同様に、一定程度見込まれることがわかった。諸外国の報告として、BA.5に対するワクチンの有効性に関する報告は非常に限られている。In vitro(試験管内)での評価として、3回接種後の血清による中和能は、BA.1/BA.2と比較してBA.4/BA.5に対して低く、ワクチンの有効性が低下する可能性が示唆された10。疫学的な暫定評価として、感染者におけるワクチン接種2回接種または3回接種のオッズがBA.1/BA.2とBA.5とで大きく変わらないという結果がイギリスやポルトガルから報告されている11-12。本調査結果では、BA.1/BA.2に対する有効性と比較して一定程度有効性が減弱する可能性が示唆されたが、信頼区間も重なっており、解釈に注意を要する。ただし、BA.5流行期においても、2回接種から半年弱後の有効性は低下した一方、ブースター接種によりワクチン有効率が高まることから、ブースター接種を検討するとともに、場面に応じた適切な感染対策を継続することが重要である。海外の報告からは、BA.1/BA.2流行期における重症化予防効果は発症予防効果よりも高い値でより長期間維持されることが報告されており、未接種者も速やかに接種を検討することが重要である11。ただし、度重なる免疫逃避能を有する変異株の出現および免疫の減衰の可能性から、オミクロン株を含めた変異株に対応したワクチンの早期の開発および導入が待たれる。
本調査は迅速な情報提供を目的としている暫定的な解析であり、今後も解析を適宜行い、経時的に評価していくことが重要である。
制 限
本調査および報告においては少なくとも以下の制限がある。まず、1つ目に交絡因子、思い出しバイアス、誤分類等の観察研究の通常のバイアスの影響を否定できない。特に、ワクチンの接種が進むにつれて、ワクチン接種者とワクチン未接種がワクチン接種歴以外の部分で異なる可能性が高くなるが、これによって起こりうる交絡として、過去の感染やマスクの着用状況、感染のリスク因子と考えられる行動の有無についても変数として解析に組み込んだ(過去の感染以外の2項目は本報告から追加)。2つ目の制限として、ワクチン接種歴等について欠損値のある者は本解析では除外している。3つ目の制限として、今回の調査は軽症例を対象としており、無症状病原体保有者・中等症例・重症例・死亡例における有効性を評価しておらず、ワクチンの種類ごとの有効性は評価していない。4つ目の制限として、本研究では陽性例についてウイルスゲノム解析を実施していない。ただし、BA.5流行期における解析であり、大部分はBA.5への感染であったとの想定のもとで実施している。5つ目の制限として、サンプルサイズの制約から有効率の信頼区間が広いため、点推定値の解釈には注意が必要である。
本調査および報告は以下の研究資金を利用して行われた:
・厚生労働科学研究費補助金「新型コロナワクチン等の有効性及び安全性の評価体制の構築に向けた研究」
・AMED新興・再興感染症に対する革新的医薬品等開発推進研究事業「ワクチンで予防可能な疾病のサーベイランス及びワクチン効果の評価に関する研究」
参考文献
- Polack FP, Thomas SJ, Kitchin N, et al. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. N Engl J Med. 2020;383(27):2603-2615. doi:10.1056/NEJMoa2034577
- Baden LR, El Sahly HM, Essink B, et al. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. N Engl J Med. 2021;384(5):403-416. doi:10.1056/NEJMoa2035389
- Voysey M, Clemens SAC, Madhi SA, et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. Lancet. 2021;397(10269):99-111. doi:10.1016/S0140-6736(20)32661-1
- 新城ら.新型コロナワクチンの有効性を検討した症例対照研究の暫定報告(第一報).国立感染症研究所.https://www.niid.go.jp/niid/ja/2019-ncov/2484-idsc/10614-covid19-55.html
- 新城ら.新型コロナワクチンの有効性を検討した症例対照研究の暫定報告(第二報):デルタ株流行期における有効性.国立感染症研究所.https://www.niid.go.jp/niid/ja/2019-ncov/2484-idsc/10757-covid19-61.html
- 新城ら.新型コロナワクチンの有効性を検討した症例対照研究の暫定報告(第三報):オミクロン株流行期における有効性.国立感染症研究所.https://www.niid.go.jp/niid/ja/2019-ncov/2484-idsc/10966-covid19-71.html
- Arashiro T, Arima Y, Muraoka H, et al. COVID-19 vaccine effectiveness against symptomatic SARS-CoV-2 infection during Delta-dominant and Omicron-dominant periods in Japan: a multi-center prospective case-control study (FASCINATE study). Clin Infect Dis. 2022;ciac635. doi:10.1093/cid/ciac635
- 厚生労働省.アドバイザリーボード資料.https://www.mhlw.go.jp/content/10900000/000972879.pdf
- 東京都総務局総合防災部防災管理課.東京都新型コロナウイルス感染症モニタリング会議・分析資料.https://www.bousai.metro.tokyo.lg.jp/taisaku/saigai/1021348/1021950.html
- Wang Q, Guo Y, Iketani S, et al. Antibody evasion by SARS-CoV-2 Omicron subvariants BA.2.12.1, BA.4, & BA.5. Nature. 2022;10.1038/s41586-022-05053-w. doi:10.1038/s41586-022-05053-w
- UK Health Security Agency. COVID-19 vaccine surveillance report (Week 31 4 August 2022). https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/1096327/Vaccine_surveillance_report_week_31_2022.pdf.
- Comparative COVID-19 Vaccines Effectiveness in Preventing Infections, Hospitalizations, and Deaths with SARS-CoV-2 BA.5 and Ba.2 Omicron Lineages: A Case-Case and Cohort Study Using Electronic Health Records in Portugal. SSRN. 2022. doi:10.2139/ssrn.4180482. https://papers.ssrn.com/sol3/papers.cfm?abstract_id=4180482.
FASCINATE study group
国立感染症研究所 感染症疫学センター 新城雄士 有馬雄三 鈴木基
クリニックフォア田町 村丘寛和
KARADA内科クリニック 佐藤昭裕
インターパーク倉持呼吸器内科 倉持仁 仁平侑希
中鉢内科・呼吸器内科クリニック 中鉢久実
聖路加国際病院 柳井敦 上原由紀 有岡宏子
国際医療福祉大学成田病院 加藤康幸
日本赤十字社医療センター 上田晃弘
公立昭和病院 大場邦弘
新宿ホームクリニック 名倉義人
複十字病院 野内英樹
町田駅前内科クリニック 伊原玄英
池袋メトロポリタン・クリニック 沼田明
横浜市立大学付属病院 加藤英明 田中克志
埼玉医科大学総合医療センター 岡秀昭 西田裕介
埼玉石心会病院 石井耕士 大木孝夫
株式会社エスアールエル
株式会社LSIメディエンス
株式会社ビー・エム・エル
株式会社ナチュラリ/東京PCR衛生検査所(所長:植島 幹九郎)
株式会社マイクロスカイラボ
株式会社みらい(代表取締役:萩原直樹)
(公表可能な医療機関・民間検査会社のみ)