2023年4月28日
国立感染症研究所
NPO法人 日本ECMOnet
端 緒
新型コロナウイルス感染症(COVID-19)に対するワクチンの開発は未曾有のスピードで進み、ファイザー社製およびモデルナ社製のmRNAワクチンは大規模なランダム化比較試験で高い有効性(vaccine efficacy)が示された1-3。国内においても、国立感染症研究所にて、複数の医療機関や民間検査会社の協力のもとで、発熱外来等で新型コロナウイルスの検査を受ける者を対象として、症例対照研究(test-negative design)を実施し、実社会における有効性(vaccine effectiveness)として、主に軽症の発症予防効果を検討してきた4-11。しかし、新型コロナワクチンの重要な効果の一つとしての重症肺炎の予防効果については国内の知見は非常に乏しかった。今回、国立感染症研究所と日本ECMOnet が共同で、デルタ流行期〜オミクロン流行初期(BA.1/BA.2流行期)における呼吸不全を伴うCOVID-19肺炎発症(中等症Ⅱ以上相当)および人工呼吸器を要するCOVID-19肺炎発症(重症相当)に対する予防効果を、症例対照研究を実施して検討することとした。
方 法
2021年8月1日から2022年6月30日までに複数の急性期病院に呼吸不全で入院した者(診断が酸素を必要とするCOVID-19肺炎、COVID-19以外の肺炎、心不全、その他呼吸器疾患等)で、16歳以上の者を対象とした。PCR、抗原検査等の検査の種類を問わず、検査陽性者を症例群(ケース)、検査陰性者を対照群(コントロール)と分類した。同一患者は初回の入院のみが組み入れられ、本解析においては、以下の者は除外して解析した:(1)発症日が不明の者、(2)発症15日以降に入院した者、(3)入院中に発症した者、(4)発症8日以上前または発症15日以降に検査された者、(5)入院15日以上前または入院15日以降に検査された者、(6)在宅酸素療法中または在宅人工呼吸器使用中の者、(7)入院15日以上前または15日以降に酸素使用を開始された者、(8)入院15日以上前または20日以降に人工呼吸器を使用開始された者、(9)3ヶ月以上前の新型コロナウイルス感染症診断歴のある者、(10)免疫不全の者または免疫抑制剤を使用している者。補足として、発症7日前以降に検査された者を組み入れ、発症8日以上前に検査された者を除外した理由は、例えば無症状スクリーニングで陽性になり、その後発症して重症化した者も含めるために発症前に検査された者も組み入れることとしたが、発症から8日以上遡ると陽性となる可能性が低くなるためである。また、入院14日前以降に検査された者を組み入れ、入院15日以上前に検査された者を除外した理由は、COVID-19においては発症後数日〜最大2週間後に重症化するため、発症直後に検査陽性となり、その後COVID-19肺炎として入院した者を含めるためである。
期間としては、2021年8月1日から2021年11月31日をデルタ流行期、2022年1月1日から2022年6月30日をオミクロン流行初期(BA.1/BA.2流行期)とした。なお、2021年12月1日から2021年12月31日に入院した症例は非流行期/置き換わり期として予防効果の推定には含めなかった。
ワクチン接種歴については、(1)未接種、(2)1回接種から13日以内、(3)1回接種から14日以降または2回接種から13日以内、(4)2回接種から14日-6ヶ月(14-181日)、(5)2回接種から6ヶ月以降(181日以降)、(6)3回接種から13日以内、(7)3回接種から14日-6ヶ月(14-181日)、(8)3回接種から6ヶ月以降(181日以降)、の8つのカテゴリーに分けた。いずれも1価ワクチン(従来株ワクチン)のみを受けた者であり、デルタ流行期は、国内において3回接種が未実施であったことからカテゴリー1-5のみとした。なお、ワクチンの最終接種日が不明の者は本解析では除外した。この影響をみるために、最終接種日不明症例も含む接種回数別の解析も行った。
ロジスティック回帰モデルを用いて、オッズ比と95%信頼区間(CI)を算出した。多変量解析における調整変数としては、先行研究等を参照し、入院時年齢群、性別、独自の重症化リスクスコア(0, 1, 2, 3, 4, 5, 6+)*、過去1年間の入院有無(自院または他院)、喫煙歴、入院医療機関の所在都府県、入院日のカレンダー週(2週ごと)をモデルに組み込んだ。ワクチン有効率は(1-調整オッズ比)×100%で推定した。
人工呼吸器を要するCOVID-19肺炎(重症相当)に対する予防効果を検討するために、症例群を、人工呼吸器を要するCOVID-19患者に限定した解析も行った(対照群については全ての呼吸不全の患者を含んでいる)。本調査は国立感染症研究所および協力医療機関において、ヒトを対象とする医学研究倫理審査で承認され、実施された(国立感染症研究所における審査の受付番号1454、1527)。
結 果
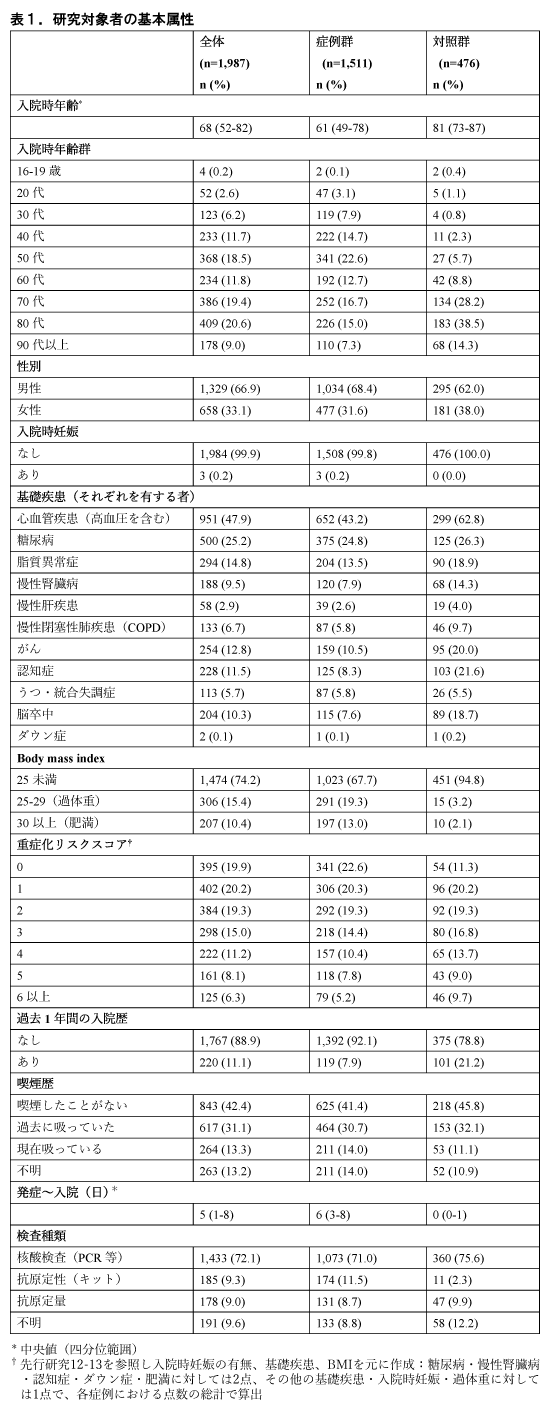
9都府県の21医療機関において、2021年8月1日から2022年6月30日までに複数医療機関に急性呼吸不全で入院した者で解析可能であった2,244名が組み入れられた。発症日が不明の者10名、発症15日以降に入院した者11名、入院中に発症した者20名、発症8日以上前または発症15日以降に検査された者41名、入院15日以上前または入院15日以降に検査された者46名、在宅酸素療法中または在宅人工呼吸器使用中の者60名、入院15日以上前または15日以降に酸素使用を開始された者10名、入院15日以上前または20日以降に人工呼吸器を使用開始された者8名、3ヶ月以上前の新型コロナウイルス感染症診断歴のある者9名、免疫不全または免疫抑制剤を使用している者42名が除外され、1987名が解析に含まれた。期間別では、デルタ流行期1025名、オミクロン流行初期(BA.1/BA.2流行期)909名、2021年12月の非流行期53名であった。解析に含まれた1,987名(うち陽性1,511名(76.0%))においては、年齢中央値(範囲)68(52-82)歳、男性1,329名(66.9%)、女性658名(33.1%)であった(表1)。ワクチンの種類(製造会社)は、全ての回で判明している者において、ファイザー社製が86.8%、モデルナ社製が7.5%、mRNAワクチンの交互接種が5.0%、その他のワクチンが0.7%であった。ワクチンの最終接種日が不明の者は217名(10.9%)であった。
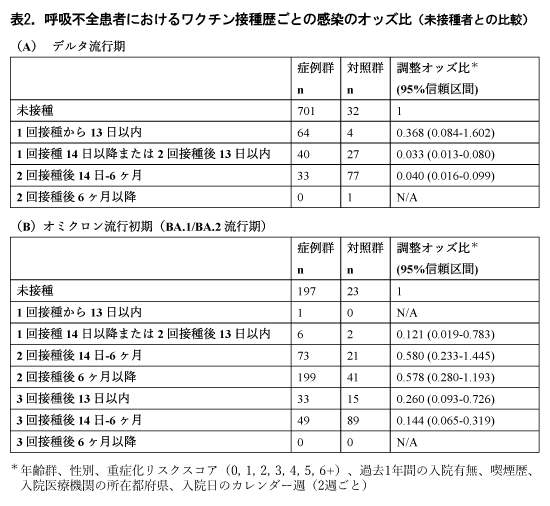
ワクチン接種歴を接種回数および接種後の期間別で8つのカテゴリーに分け、検査陽性者(症例群)と検査陰性者(対照群)とで比較した(表2、表3)。
呼吸不全患者において、未接種者を参照項とする調整オッズ比は、デルタ流行期における2回接種後14日-6ヶ月では0.040 (95%CI 0.016-0.099)(表2A)、オミクロン流行初期における2回接種後6ヶ月以降では0.578 (95%CI 0.280-1.193)、ブースター(3回目)接種後14日-6ヶ月では0.144 (95%CI 0.065-0.319)であった(表2B)。
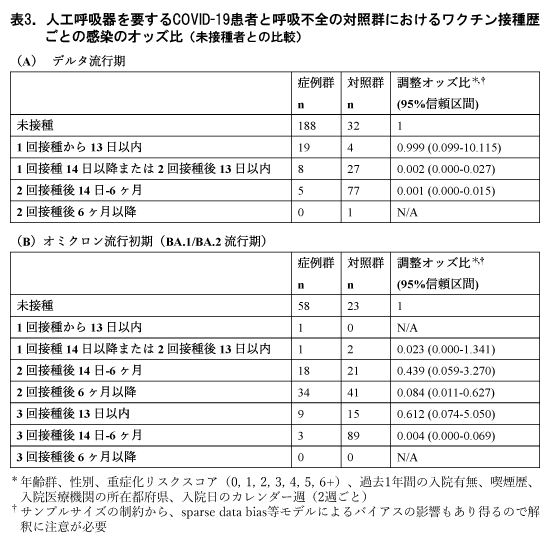
人工呼吸器を要するCOVID-19患者と呼吸不全の対照群において、未接種者を参照項とする調整オッズ比は、デルタ流行期における2回接種後14日-6ヶ月では0.001 (95%CI 0.000-0.015) (表3A)、オミクロン流行初期における2回接種後6ヶ月以降では0.084 (95%CI 0.011-0.627)、3回接種後14日-6ヶ月では0.004 (95%CI 0.000-0.069)であった(表3B)。なお、サンプルサイズの制約から、sparse data bias等モデルによるバイアスの影響もあり得るので解釈に注意が必要である。
最終接種日不明症例も含む接種回数別の解析でも類似の結果であった。
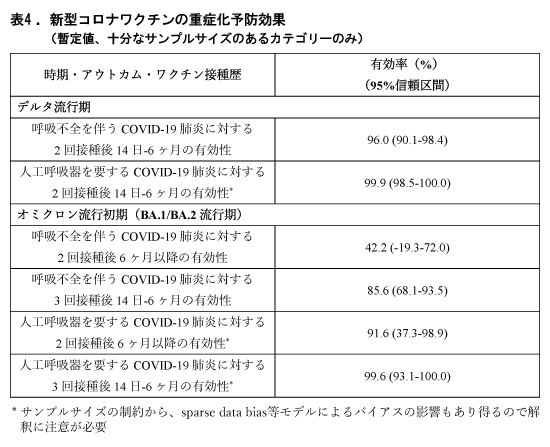
調整オッズ比を元にワクチン有効率を算出したところ、デルタ流行期において、呼吸不全を伴うCOVID-19肺炎に対する2回接種後14日-6ヶ月の有効性は96.0% (95%CI 90.1-98.4%)、人工呼吸器を要するCOVID-19肺炎に対する2回接種後14日-6ヶ月の有効性は99.9% (95%CI 98.5-100.0%)であった(表4)。また、オミクロン流行初期においては、呼吸不全を伴うCOVID-19肺炎に対する2回接種後6ヶ月以降の有効性は42.2% (95%CI -19.3-72.0%)、3回接種後14日-6ヶ月の有効性は85.6% (95%CI 68.1-93.5%)であり、人工呼吸器を要するCOVID-19肺炎に対する2回接種後6ヶ月以降の有効性は91.6% (95%CI 37.3-98.9%)、3回接種後14日-6ヶ月の有効性は99.6% (95%CI 93.1-100.0%)であった(表4)。
考 察
本報告では、デルタ流行期〜オミクロン流行初期(BA.1/BA.2流行期)における呼吸不全を伴うCOVID-19肺炎および人工呼吸器を要するCOVID-19肺炎に対する予防効果を検討した。デルタ流行期においては、呼吸不全を伴うCOVID-19肺炎および人工呼吸器を要するCOVID-19肺炎に対して、ともに非常に高い有効性(点推定値:それぞれ96%、>99%)を示した。
オミクロン流行初期においては、2回接種後6ヶ月以降で、呼吸不全を伴うCOVID-19肺炎に対しては低下したが(点推定値:42%)、人工呼吸器を要するCOVID-19肺炎に対しては高い有効性(点推定値:92%)であった(ともに信頼区間が広く解釈に注意が必要)。また、ブースター(3回目)接種により、呼吸不全を伴うCOVID-19肺炎および人工呼吸器を要するCOVID-19肺炎に対して、ともに有効性が高まった(点推定値:それぞれ86%、>99%)。
諸外国においては、入院予防効果を検討した研究結果が数多く報告されている14-15。国内で承認されているワクチンにおいて、デルタ流行期には、一貫して高い重症化予防効果が示されてきた14。しかし、オミクロン流行期においては、2回接種およびブースター接種において、50-100%と幅のある重症化予防効果が報告されている15。本報告においては、COVID-19重症肺炎により特異的なアウトカム(転帰)である酸素需要を伴う症例や人工呼吸器を要する症例に限定して解析を行うことで、より確度の高い推定を目指した16。オミクロン流行期においては、入院患者で偶発的に新型コロナウイルス感染者が増えており、入院予防効果では有効性を過小評価しうるため、この考慮は特に重要となる。
本報告では、デルタ流行期における2回接種の高い重症化予防効果、オミクロン流行初期における3回接種の高い重症化予防効果が示された。2023年5月からCOVID-19の感染症法上の位置づけは5類感染症へ移行するが、今後も、有効性や安全性等のエビデンスに基づいて新型コロナワクチンの接種戦略を検討することが重要となる。
制 限
本調査および報告においては少なくとも以下の制限がある。まず、1つ目に交絡因子、誤分類等の観察研究の通常のバイアスの影響を否定できない。2つ目の制限として、上述の通り、ワクチンの最終接種日が不明の者(10.9%)は本解析では除外している。ただし、最終接種日不明症例も含む接種回数別の解析を行ったところ、類似の結果であった。3つ目の制限として、今回の調査では、ワクチンの製造会社ごとの有効性は評価していない。4つ目の制限として、本研究では陽性例についてウイルスゲノム解析を実施していない。ただし、デルタ流行期、オミクロン流行初期における解析であり大部分はそれぞれデルタ、BA.1/BA.2への感染であったとの想定のもとで実施している。5つ目の制限として、サンプルサイズの制約から、一部の推定では有効率の信頼区間が広いため、点推定値の解釈には注意が必要である。なお、人工呼吸器を要する症例と呼吸不全の対照群を比較した調整オッズ比は、点推計値が過大評価されている可能性(sparse data bias)があるが、この二群におけるワクチン接種歴の分布は大きく異なっていた。6つ目の制限として、3回接種の中長期的な重症化予防効果、4回接種およびオミクロン対応2価ワクチンの重症化予防効果は検討しておらず、これらは今後の検討課題である。
本調査および報告は以下の研究資金を利用して行われた:
参考文献
- Polack FP, Thomas SJ, Kitchin N, et al. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. N Engl J Med. 2020;383(27):2603-2615. doi:10.1056/NEJMoa2034577
- Baden LR, El Sahly HM, Essink B, et al. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. N Engl J Med. 2021;384(5):403-416. doi:10.1056/NEJMoa2035389
- Voysey M, Clemens SAC, Madhi SA, et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. Lancet. 2021;397(10269):99-111. doi:10.1016/S0140-6736(20)32661-1
- 新城ら.新型コロナワクチンの有効性を検討した症例対照研究の暫定報告(第一報).国立感染症研究所.https://www.niid.go.jp/niid/ja/2019-ncov/2484-idsc/10614-covid19-55.html
- 新城ら.新型コロナワクチンの有効性を検討した症例対照研究の暫定報告(第二報):デルタ株流行期における有効性.国立感染症研究所.https://www.niid.go.jp/niid/ja/2019-ncov/2484-idsc/10757-covid19-61.html
- 新城ら.新型コロナワクチンの有効性を検討した症例対照研究の暫定報告(第三報):オミクロン株流行期における有効性.国立感染症研究所.https://www.niid.go.jp/niid/ja/2019-ncov/2484-idsc/10966-covid19-71.html
- Arashiro T, Arima Y, Muraoka H, et al. COVID-19 vaccine effectiveness against symptomatic SARS-CoV-2 infection during Delta-dominant and Omicron-dominant periods in Japan: a multi-center prospective case-control study (FASCINATE study). Clin Infect Dis. 2022;ciac635. doi:10.1093/cid/ciac635
- 新城ら.新型コロナワクチンの有効性を検討した症例対照研究の暫定報告(第四報):オミクロン株(BA.1/BA.2およびBA.5)流行期における有効性.国立感染症研究所.https://www.niid.go.jp/niid/ja/2019-ncov/2484-idsc/11405-covid19-999.html
- 新城ら.新型コロナワクチンの有効性を検討した症例対照研究の暫定報告(第五報):オミクロン対応2価ワクチンの有効性.国立感染症研究所.https://www.niid.go.jp/niid/ja/2019-ncov/2484-idsc/11688-covid19-9999.html
- Arashiro T, Arima Y, Kuramochi J, et al. Importance of considering high-risk behaviours in COVID-19 vaccine effectiveness estimates with observational studies. Euro Surveill. 2023;28(4):2300034. doi:10.2807/1560-7917.ES.2023.28.4.2300034
- Arashiro T, Arima Y, Kuramochi J, et al. Effectiveness of BA.1- and BA.4/BA.5-containing bivalent COVID-19 mRNA vaccines against symptomatic SARS-CoV-2 infection during the BA.5-dominant period in Japan. Open Forum Infect Dis. doi:10.1093/ofid/ofad240 (Editor’s Choice)
- Williamson EJ, Walker AJ, Bhaskaran K, et al. Factors associated with COVID-19-related death using OpenSAFELY. Nature. 2020;584(7821):430-436.
- Clift AK, Coupland CAC, Keogh RH, et al. Living risk prediction algorithm (QCOVID) for risk of hospital admission and mortality from coronavirus 19 in adults: national derivation and validation cohort study. BMJ. 2020;371:m3731. Published 2020 Oct 20. doi:10.1136/bmj.m3731
- International Vaccine Access Center (IVAC), Johns Hopkins Bloomberg School of Public Health. VIEW-hub: COVID-19 data, vaccine effectiveness studies. https://view-hub.org/covid-19/effectiveness-studies.
- Feikin DR, Higdon MM, Abu-Raddad LJ, et al. Duration of effectiveness of vaccines against SARS-CoV-2 infection and COVID-19 disease: results of a systematic review and meta-regression. Lancet. 2022;399(10328):924-944.
- World Health Organization. Evaluation of COVID-19 vaccine effectiveness in a changing landscape of COVID-19 epidemiology and vaccination: interim guidance, 1 October 2022: second addendum to Evaluation of COVID-19 vaccine effectiveness: interim guidance. https://apps.who.int/iris/handle/10665/363344
MOTIVATE study group
国立感染症研究所 感染症疫学センター 新城雄士 有馬雄三 鈴木基NPO法人 日本ECMOnet/かわぐち心臓呼吸器病院 竹田晋浩
NPO法人 集中治療コラボレーションネットワーク/NPO法人 日本ECMOnet 橋本悟
NPO法人日本ECMOnet/大阪大学医学部附属病院 藤野裕士
東京都立広尾病院 三輪槙 中西明日香
大阪市立総合医療センター 中河秀憲 林下浩士
関西労災病院 髙松純平
公立昭和病院 大場邦弘 谷山大輔
大阪急性期・総合医療センター 藤見聡 山口浅瀬
相模原協同病院 菊地斉
横須賀市立うわまち病院 岩澤孝昌 内倉淑男
上尾中央総合病院 神部芙美子
かわぐち心臓呼吸器病院 大山慶介
東京警察病院 金井尚之 松永麻衣子
八尾徳洲会総合病院 緒方嘉隆 濵口眞成 元田健太郎
北里大学北里研究所病院 朝倉崇徳 中山莊平
佐野厚生総合病院 浅見貴弘
順天堂大学医学部附属練馬病院 杉田学 水野慶子
聖路加国際病院 仁多寅彦
埼玉医科大学総合医療センター 岡秀昭 西田裕介 山本慧
横浜市立大学附属病院 加藤英明 田中克志
奈良県総合医療センター 安宅一晃 日垣太希
紀南病院 中野好夫
東京大学医学部附属病院 堤武也 土井研人 奥川周
日本赤十字社医療センター 上田晃弘
総合病院国保旭中央病院 中村朗 井上武 小林三枝子
聖マリアンナ医科大学病院 藤谷茂樹 吉田徹
東京都立多摩総合医療センター 清水敬樹 三森薫
秋田赤十字病院 藤田康雄
東京山手メディカルセンター 大河内康実
京都市立病院 栃谷健太郎
本調査にご協⼒いただいた上記医療機関の職員皆様、技術/事務的支援をしていただいた以下の会社の皆様および研究補助員の皆様に⼼より御礼申し上げます:
株式会社アクセライズ・サイト、レバレジーズメディカルケア株式会社、株式会社うるるBPO、瑞穂印刷株式会社、千木良望、淺野瑠々実、塚原万葵、竹田早希
注意事項
迅速な情報共有を⽬的とした暫定的な資料であり、内容や⾒解は知見の更新によって変わる可能性がある。