お知らせ
感染症情報
研究・検査・病原体管理
サーベイランス
刊行・マニュアル・基準
- 詳細
平成19年12月28日
| 都道府県 | ||
| 各 | 政令市 | 衛生主管部(局)長 殿 |
| 特別区 |
感染症の予防及び感染症の患者に対する医療に関する法律施行規則の一部を改正する省令(平成19年厚生労働省令第159号)が平成19年12月28日公布され、平成20年1月1日に施行されること等に伴い「感染症の予防及び感染症の患者に対する医療に関する法律第12条第1項及び第14条第2項に基づく届出の基準等について」(平成18年3月8日健感発第0308001号)の一部を下記のとおり改正し、同日から適用する。
- 詳細
感染症の予防及び感染症の患者に対する医療に関する法律及び検疫法の一部を改正する法律(平成20年法律30号)は、2008(平成20)年5月2日に公布され、5月12日から施行されている(http://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou04/16.html)。
- 詳細
|
〈第14週コメント〉 4月11日集計分 ◆全数報告の感染症 注意:これは当該週に診断された報告症例の集計です。しかし、迅速に情報還元するために期日を決めて集計を行いますので、当該週に診断された症例の報告が集計の期日以降に届くこともあります。それらについては一部を除いて発生動向総覧では扱いませんが、翌週あるいはそれ以降に、巻末の表の累積数に加えられることになります。 *感染経路、感染原因、感染地域については、確定あるいは推定として記載されていたものを示します。
全国の指定された医療機関(定点)から報告され、疾患により小児科定点(約3,000 カ所)、インフルエンザ(小児科・内科)定点(約5,000 カ所)、眼科定点(約600 カ所)、基幹定点(約500 カ所)に分かれています。また、定点当たり報告数は、報告数/定点医療機関数です。
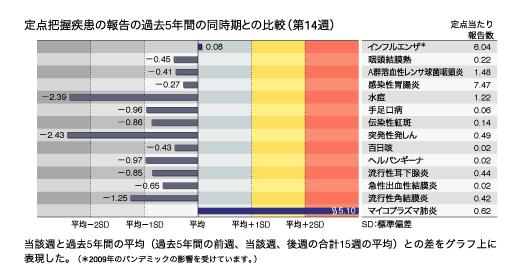
インフルエンザ:定点当たり報告数は第6週以降減少が続いている。都道府県別では福井県(20.88)、福島県(13.60)、鳥取県(12.17)、山形県(10.42)、新潟県(9.87)が多い。 小児科定点報告疾患:RSウイルス感染症の報告数は678例と第11週以降減少が続いている。年齢別では1歳以下の報告数が全体の約80%を占めている。咽頭結膜熱の定点当たり報告数は2週連続で増加した。都道府県別では富山県(0.83)、福岡県(0.82)、鹿児島県(0.49)が多い。A群溶血性レンサ球菌咽頭炎の定点当たり報告数は第11週以降減少が続いている。都道府県別では富山県(4.76)、鳥取県(4.58)、大分県(4.14)が多い。感染性胃腸炎の定点当たり報告数は2週連続で増加した。都道府県別では愛媛県(14.8)、大分県(13.5)、福岡県(12.5)が多い。水痘の定点当たり報告数は2週連続で減少した。都道府県別では宮崎県(3.58)、石川県(2.46)、鹿児島県(2.44)が多い。手足口病の定点当たり報告数は減少した。都道府県別では沖縄県(0.94)、石川県(0.68)、福井県(0.50)が多い。伝染性紅斑の定点当たり報告数は減少した。都道府県別では鳥取県(0.84)、徳島県(0.70)、高知県(0.60)が多い。百日咳の定点当たり報告数は2週連続で増加した。都道府県別では高知県(0.30)、沖縄県(0.18)、福岡県(0.06)が多い。ヘルパンギーナの定点当たり報告数は減少した。都道府県別では宮崎県(0.22)、熊本県(0.15)、富山県(0.10)が多い。流行性耳下腺炎の定点当たり報告数は減少した。都道府県別では大分県(1.72)、宮崎県(1.25)、宮城県(1.10)が多い。 基幹定点報告疾患:マイコプラズマ肺炎の定点当たり報告数は第11週以降減少が続いているが、過去5年間の同時期(前週、当該週、後週)と比較してかなり多い。都道府県別では沖縄県(3.14)、福島県(2.00)、埼玉県(1.78)が多い。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
- 詳細
わが国におけるブルーリ潰瘍の臨床例
(IASR Vol. 33 p. 91-93: 2012年4月号)
岡山大学皮膚科では2008年より、8歳女児・10歳女児・73歳男性・49歳女性の4例のブルーリ潰瘍症例を経験した。いずれも契機となる外傷や虫刺は明らかでなく、海外への渡航歴や家族に同症をみとめない。発症部位と皮疹の性状は、下腿が3例・上腕が1例で、すべて単発の潰瘍を伴った病変であった。本稿では当科での症例を提示し、岡山県内の他施設からの症例も加えて県内での発症状況(2011年末までで8症例)について考察した。
症例提示 8歳 女児(図1)
主訴:右外果部の潰瘍、疼痛
初診: 2008年1月15日
既往歴・家族歴:特記すべき事項なし
生活歴:小学生、岡山県南部在住、渡航歴なし
現病歴:2007年12月頃右外果に靴擦れ様の皮疹出現。近医よりセフジトレンピボキシルを投与されたが改善せず。2008年1月に近医皮膚科を受診し蜂窩織炎疑いで、セフジニル、ホスホマイシンを内服するも無効。発赤腫脹が下腿に拡大し精査目的で当科を紹介受診した。
現症:発熱なし、倦怠感なし。右外果から踵部にかけて境界不明瞭な紅暈を伴った、黄色調の壊死組織を付す5.5×4cm大の潰瘍をみとめた(図1A)。
臨床検査所見:WBC 6,940/μl (Ne 48.8、Ly 44.7、Mo 4.6、Eo1.7、Bas 0.3)、RBC 5.26×106/μl、Hb 14.1 g/dl、Ht 42.5%、Plt 3.24×105 /μl、AST 29 U/l、ALT 18 U/l、LDH 230 IU/l、CRP 0.13mg/dl、クォンティフェロン陰性
胸部X-p:活動性病変なし
抗酸菌塗抹:Gaffky 10号陽性
病理組織像:潰瘍辺縁を紡錐形に生検した。HE染色では真皮から脂肪織が壊死におちいり、散在性に好中球・リンパ球様単核球が浸潤し、明らかな肉芽腫の形成をみとめなかった。
治療と経過:非結核性抗酸菌症と考えてクラリスロマイシンの内服を開始。周囲の紅暈は消退し潰瘍も縮小したが完全には上皮化しなかった。数回施行した潰瘍底のスメアでも抗酸菌陽性(Gaffky 2~5号)で、同定依頼(福島県立医科大学微生物学教室:錫谷達夫先生)の結果、Mycobacterium ulcerans subsp. shinshuense と同定された(図1B、C)。内服治療に抵抗性で、デブリードマンを施行しつつ経過観察するも潰瘍が持続した。入院の上、4月15日に全身麻酔下でデブリードマンと表皮移植術を施行し瘢痕治癒した(図1D、E)。
当科での症例について(図2)
図2は当科経験症例の臨床像である。4症例中3例は女児ないし女性に発症し、下腿の単発性病変で潰瘍を形成していた。病理組織学的には全例で真皮から脂肪織にいたる広汎な壊死像で肉芽腫の形成をみとめなかった。3例とも抗菌薬の投与と外科的デブリードマンまたは切除をおこなった。10歳女児症例では画像上筋膜まで病変をみとめたために、筋膜をつけて全切除した。残りの1例は高齢の男性の上腕に生じ筋層の変性を伴った症例で、筋切除によるADL 低下が懸念されたために、保存的に治療し軽快している。
岡山県内での発症状況(図3)
上述の4症例に、岡山県内の他施設(川崎医科大学、岡山医療センター、川崎医科大学附属川崎病院)の4症例を加えて岡山県内で発症した症例の特徴を検討した。初診時年齢は8~73歳で中央値が49歳、年齢分布では19歳までの若年層とともに40~59歳にもピークがあった。男女比は0.33で女性に多かった(図3A)。病変は四肢、特に下腿に好発し(50%)、8症例中6例が単発性であった(図3B)。病変は潰瘍形成をしばしば伴い、50%が有痛性であった(図3C)。治療では全例に抗菌薬が使用され、ミノサイクリン(75%)、レボフロキサシン(38%)、クラリスロマイシン(38%)など、複数の抗菌薬と手術療法(75%)がしばしば施行されていた。転帰は経過の追えた7症例中6例(86%)が治癒、1例(14%)が軽快した(図3D)。発症症例の居住地は県南部の内陸部に多かった。
岡山大学医学部皮膚科 濱田利久
- 詳細
ブルーリ潰瘍の検査
(IASR Vol. 33 p. 93-94: 2012年4月号)
ブルーリ潰瘍の検査に必要なサンプルは、基本的には一般細菌感染症と同様で、抗菌薬治療の前に採取すべきである。ブルーリ潰瘍のみならず、一般細菌感染の疑いがある場合には、綿棒で潰瘍底などの皮疹部をこすり(swab)、あるいは浸出液や膿汁、さらに生検皮膚組織などをサンプルとして用いる。初期の検査で診断がつかず、再度の検体入手が困難な場合でも、病理組織標本のパラフィンブロックが保存されていれば、PCRによるブルーリ潰瘍スクリーニング検査のサンプルとして使用できる。また、小川培地での培養に成功し、鑑別同定する場合、その菌、あるいは抽出したDNAもサンプルとして用いられる。表1にはサンプルとその処理方法についてまとめた。
検査でわかること
a)抗酸菌の有無
スタンプ標本検査、あるいは病理組織検査で、チール・ニールセン(Z-N)染色により抗酸菌を検出する。Mycobacterium ulcerans subsp. shinshuense は、比較的菌体が短い特徴があるが、菌種の識別はできない。
b)M. ulcerans/M. ulcerans subsp. shinshuense とM. marinum との鑑別
PCR法によってM. ulcerans およびM. ulcerans subsp. shinshuense に特異的なインサージョンシークエンス(IS)2404 を検出する(図1)。全長が1,274bpのIS2404 の154bpを標的にしたPCR法は感度が高く、サイズが短いためパラフィン切片サンプルからも検出できる。ただし、魚病由来のM. pseudoshotosii などヒト以外でIS2404 陽性となる菌種も知られているので、環境調査の際には注意が必要である。
c)M. ulcerans とM. ulcerans subsp. shinshuense の鑑別
16S rRNA遺伝子検査を行い、特に3´末端のシークエンスを比較する。これまでの日本の症例や中国の症例はすべて、M. ulcerans subsp. shinshuense であった。
ブルーリ潰瘍確定診断検査のフローチャート図2を示した。培養検査は長期間を要するが、薬剤感受性検査や詳細な細菌学的検査を行うためには非常に重要である。培養11カ月でようやく培養に成功した例もあるので、25℃(室温)~34℃で、少なくとも3カ月は培養を続ける。あるいは国立感染症研究所ハンセン病研究センターへ、培養を委託することも可能である。
おわりに
日本ではこれまでブルーリ潰瘍の報告が少なく、認知度が低いため、ブルーリ潰瘍の検査が行われずに、慢性化してしまう症例が多かった。いったん症例を経験した施設では、早期の適切なサンプル採取により培養検査にも成功する場合が多い。今後この疾患を多くの人が知ることで、早期の検査で診断、治療が迅速に行われるであろう。
参考文献
1) WHO, Buruli ulcer: diagnosis of Mycobacterium ulcerans disease: amanual for health careproviders, 2001
(http://whqlibdoc.who.int/hq/2001/WHO_CDS_CPE_GBUI_2001.4.pdf)
2) Nakanaga K, et al ., J Clin Microbiol 49: 3829-3836, 2011
3) Portaels F, et al ., J Clin Microbiol 34: 962-965, 1996
4) Nakanaga K, et al ., J Clin Microbiol 45: 3840-3843, 2007
国立感染症研究所ハンセン病研究センター感染制御部 中永和枝
- 詳細
Mycobacterium ulcerans の産生するマイコラクトン
ブルーリ潰瘍にみられる痛みのない(少ない)皮膚潰瘍では、皮膚・皮下組織に特徴的な病変が認められる。すなわち、脂肪組織を中心とした広範な壊死があるにもかかわらず、一般の脂肪壊死で観察されるマクロファージや好中球などの炎症細胞がほとんどみられず、fat cell ghostと表現されている。古くなった線維化病変でも細胞核はまばらにしかみられない。これらの病変は菌の分布を超えて広い範囲にみられることから、病変の形成にはMycobacterium ulcerans が産生して菌外に分泌する毒素の存在が示唆されていた。その後の研究によって、毒性脂質のマイコラクトン(mycolactone)が関与していることが明らかになった。
マイコラクトンの構造と産生、測定法
マイコラクトンはマクロライドに属する化合物で、二つのポリケチド鎖(ラクトン核)のエステル結合によって作られる(図)。これらのラクトン核は、M. ulcerans の巨大プラスミドpMUM001にコードされているポリケチド合成酵素(Pks)によって合成される。M. ulcerans (subsp. shinshuense を含む)以外にも、類縁抗酸菌であるM. liflandii 、M. pseudoshottsii と一部のM. marinum がマイコラクトンを産生することが知られている。マイコラクトンには脂肪酸側鎖の種類によってA/B ~Gまでの構造亜型があり、アフリカのM. ulcerans とM. ulcerans subsp. shinshuense はA/B(分子式 C44H70O9)を、オーストラリアのM. ulcerans はCを、アフリカツメガエルのM. liflandii はEを、魚のM. marinum はFを産生する。
マイコラクトンはプラスミドの遺伝子によって合成されることから、菌がプラスミドを失えばマイコラクトンは産生されなくなる。精製したマイコラクトンは黄色であるが、中永によると、M. ulceransの培養コロニーは継代培養中にしばしば黄色から白色に変異し、マイコラクトン産生能と細胞毒性を消失する。
岸 義人らはマイコラクトンの人工合成を行い、我々の実験(未発表)では合成マイコラクトンは精製マイコラクトンとほぼ同等の生物活性を示している。
病変組織あるいは血清から脂質を抽出し、高速液体クロマトグラフィーと質量分析の組み合わせでマイコラクトンを検出することができる。現時点では、精度の高い簡易測定法は報告されていない。
マイコラクトンの生物活性
マイコラクトンは毒性脂質であり、線維芽細胞、脂肪細胞、マクロファージ、角化細胞などに対して、用量依存性に壊死とアポトーシスの両方の機序による細胞傷害性があり、細胞を壊死させるために皮膚潰瘍を形成する。マイコラクトンが末梢神経のシュワン細胞も障害するために、潰瘍になっても痛み刺激に対する閾値が最終的に低下することを、我々は動物実験で明らかにした。マイコラクトンは側鎖構造によって生物活性が異なり、亜型の中ではA/Bが最も強い細胞毒性を示す。
マイコラクトンは免疫抑制作用も持っている。ブルーリ潰瘍患者の末梢血単核細胞では、細胞毒性よりはるかに低濃度でIFN-γ産生が抑制され、IL-4優位のTh2サイトカインパターンを示すことがわかっている。
参考文献
1) George KM, et al ., Science 283: 854-857, 1999
2) Hong H, et al ., Nat Prod Rep 25: 447-454, 2008
3) Kishi Y, PNAS 108: 6703-6708, 2011
4) Sarfo FS, et al ., PLoS Negl Trop Dis 5: e1237, 2011
5) En J, et al ., Infect Immun 76: 2002-2007, 2008
国立療養所星塚敬愛園 後藤正道