お知らせ
感染症情報
研究・検査・病原体管理
サーベイランス
刊行・マニュアル・基準
- 詳細
| 【速報一覧へ戻る】 | |
ブタの日本脳炎抗体保有状況 -2013年速報第3報-(2013年8月2日現在) |
|
| 日本脳炎は,日本脳炎ウイルスに感染したヒトのうち数百人に一人が発症すると考えられている重篤な脳炎である1)。ヒトへの感染は,日本脳炎ウイルスを媒介する蚊(日本では主にコガタアカイエカ)が日本脳炎ウイルスに感染したブタを吸血し,その後ヒトを刺すことにより起こる。 1960年代までは毎年夏から秋にかけて多数の日本脳炎患者が発生しており2),3),ブタの感染状況から日本脳炎ウイルスが蔓延している地域に多くの患者発生がみられた。当時,Konnoらは調査したブタの半数以上が日本脳炎ウイルスに感染していると,約2週間後からその地域に日本脳炎患者が発生してくると報告している4)。現在では,日本脳炎ワクチン接種の普及や生活環境の変化等により,ブタの感染状況と患者発生は必ずしも一致しておらず,近年における日本脳炎患者報告数は毎年数名程度である。しかし,ブタの抗体保有状況から日本脳炎ウイルスが蔓延あるいは活動していると推測される地域では,ヒトへの感染の危険性が高くなっていることが考えられる。 感染症流行予測調査事業では,全国各地のブタ血清中の日本脳炎ウイルスに対する抗体を赤血球凝集抑制法(HI法)により測定することで,日本脳炎ウイルスの蔓延状況および活動状況を調査している。前年の秋以降に生まれたブタが日本脳炎ウイルスに対する抗体を保有し,さらに2-メルカプトエタノール(2-ME)感受性抗体(IgM抗体)を保有している場合,そのブタは最近日本脳炎ウイルスに感染したと考えられる。下表は本年度の調査期間中におけるブタの抗体保有状況について都道府県別に示しており,日本脳炎ウイルスの最近の感染が認められた地域を青色,それに加えて調査したブタの50%以上に抗体保有が認められた地域を黄色,調査したブタの80%以上に抗体保有が認められた地域を赤色で示している。 本速報は日本脳炎ウイルスの感染に対する注意を喚起するものである。また,それぞれの居住地域における日本脳炎に関する情報にも注意し,日本脳炎ウイルスが蔓延あるいは活動していると推測される地域においては,予防接種を受けていない者,乳幼児,高齢者は蚊に刺されないようにするなど注意が必要である。 本年度の日本脳炎定期予防接種は,第1期(3回)については標準的な接種年齢である3~4歳および第1期接種が完了していない小学1~4年生(年度内に7~10歳:2003~2006年度生まれ),第2期(1回)については高校3年生相当年齢(年度内に18歳:1995年度生まれ)に積極的勧奨が行われているが,それ以外でも日本脳炎ウイルスの活動が活発な地域に居住し,接種回数が不十分な者は日本脳炎ワクチンの接種が望まれる。なお,日本脳炎の予防接種に関する情報については以下のサイトから閲覧可能である。 【 国立感染症研究所HP / 厚生労働省HP 】 |
抗体保有状況 (地図情報) 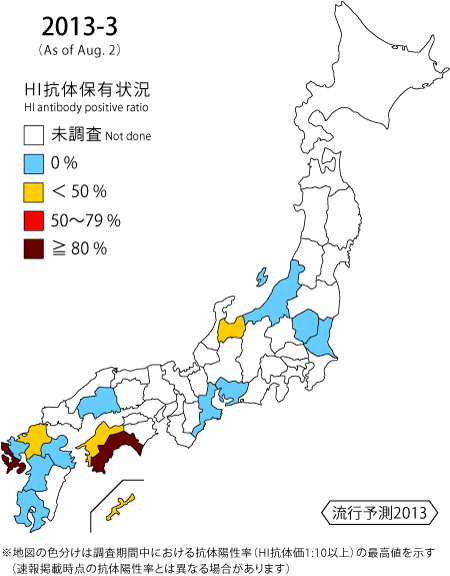 抗体保有状況 (月別推移) 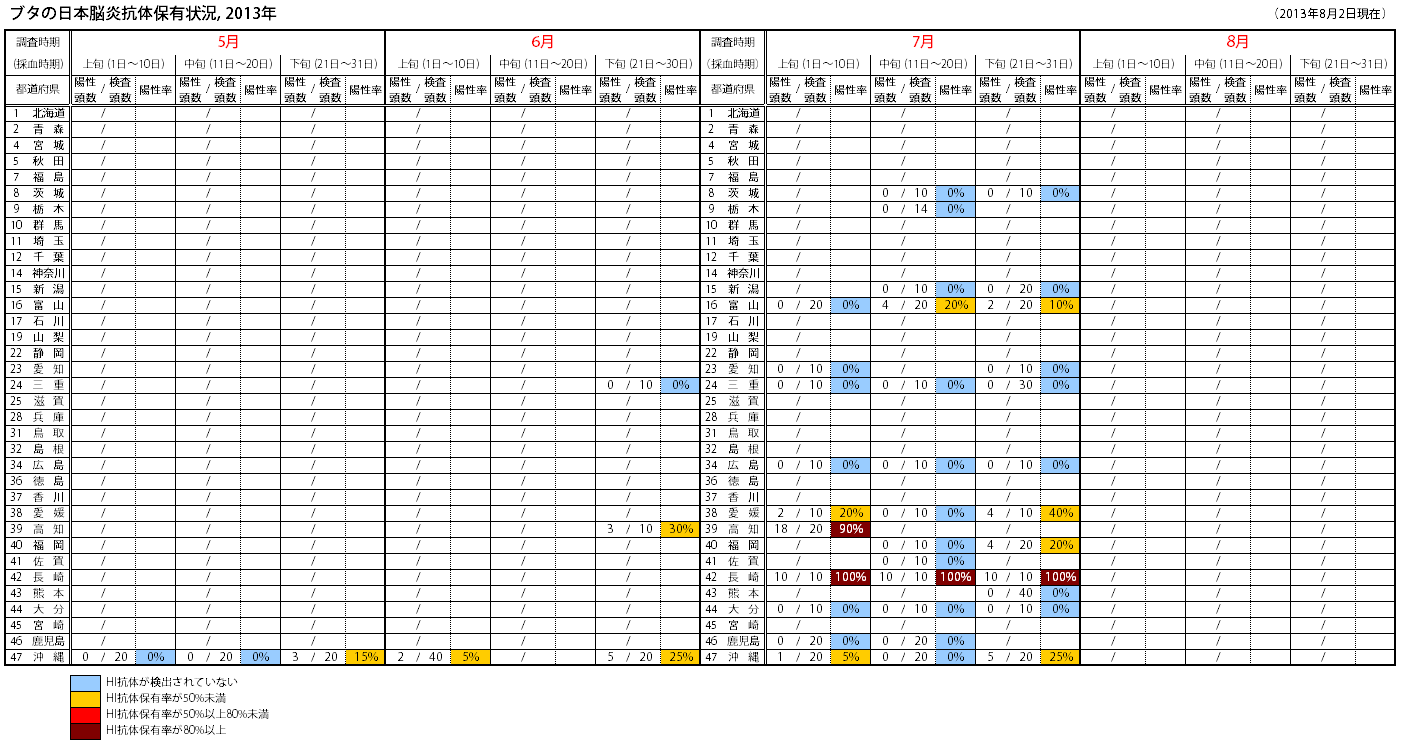
|
| HI抗体 | 2-ME 感受性 抗体 |
都道府県 | 採血 月日 |
HI抗体 陽性率 ※1 |
2-ME感受性 抗体陽性率 ※2 |
コメント |
| ◎ 5/27 |
◎ 6/24 |
沖縄県 | 7/29 | 25% (5/20) |
50% (2/4) |
HI抗体陽性例のうち4頭は抗体価1:40以上であり、そのうち2頭から2-ME感受性抗体が検出された。 |
| |
|
鹿児島県 | 7/16 | 0% (0/20) |
|
|
| |
|
大分県 | 7/22 | 0% (0/10) |
|
|
| |
|
熊本県 | 7/29 | 0% (0/20) |
|
|
| ◎ 7/2 |
|
長崎県 | 7/23 | 100% (10/10) |
0% (0/1) |
HI抗体陽性例のうち1頭は抗体価1:40以上であったが、2-ME感受性抗体は検出されなかった。 |
| |
|
佐賀県 | 7/17 | 0% (0/10) |
|
|
| ◎ 7/23 |
◎ 7/23 |
福岡県 | 7/30 | 30% (3/10) |
100% (3/3) |
HI抗体陽性例はすべて抗体価1:40以上であり、2-ME感受性抗体も検出された。 |
| ◎ 6/25 |
◎ 6/25 |
高知県 | 7/9 | 90% (9/10) |
50% (4/8) |
HI抗体陽性例のうち8頭は抗体価1:40以上であり、そのうち4頭から2-ME感受性抗体が検出された。 |
| ◎ 7/9 |
◎ 7/23 |
愛媛県 | 7/23 | 40% (4/10) |
100% (4/4) |
HI抗体陽性例はすべて抗体価1:40以上であり、2-ME感受性抗体も検出された。 |
| |
|
広島県 | 7/24 | 0% (0/10) |
|
|
| |
|
三重県 | 7/29 | 0% (0/10) |
|
|
| |
|
愛知県 | 7/22 | 0% (0/10) |
|
|
| ◎ 7/16 |
|
富山県 | 7/22 -23 |
10% (2/20) |
|
HI抗体陽性例はすべて抗体価1:40未満であった。 |
| |
|
新潟県 | 7/30 | 0% (0/10) |
|
|
| |
|
栃木県 | 7/16 | 0% (0/14) |
|
|
| |
|
茨城県 | 7/29 | 0% (0/10) |
|
|
| 調査期間中に調査したブタのHI抗体陽性率が80%を超えた地域 | ||||||
| 調査期間中に調査したブタのHI抗体陽性率が50%を超え,かつ2-ME感受性抗体が検出された地域 | ||||||
| 調査期間中に調査したブタから2-ME感受性抗体が検出された地域 | ||||||
| ◎ | 調査期間中に調査したブタからHI抗体あるいは2-ME感受性抗体が検出されたことを示し、日付は今シーズンで初めて検出された採血月日を示す | |||||
| ※1 HI抗体は抗体価1:10以上を陽性と判定した。 ※2 2-ME感受性抗体は抗体価1:40以上(北海道・東北地方は1:10以上)の検体について検査を行い,2-ME処理を行った血清の抗体価が未処理の血清と比較して,3管(8倍)以上低かった場合を陽性,2管(4倍)低かった場合を疑陽性,不変または1管(2倍)低かった場合を陰性と判定した。なお,2-ME未処理の抗体価が1:40(北海道・東北地方は1:10あるいは1:20も含む)で,2-ME処理後に1:10未満となった場合も陽性と判定した。 |
||||||
| 1. | Southam, C. M., Serological studies of encephalitis in Japan. II. Inapparent infection by Japanese B encephalitis virus. Journal of Infectious diseases. 1956. 99: 163-169. |
| 2. | 松永泰子,矢部貞雄,谷口清州,中山幹男,倉根一郎. 日本における近年の日本脳炎患者発生状況-厚生省伝染病流行予測調査および日本脳炎確認患者個人票(1982~1996)に基づく解析-. 感染症学雑誌. 1999. 73: 97-103. |
| 3. | 新井 智,多屋馨子,岡部信彦,高崎智彦,倉根一郎. わが国における日本脳炎の疫学と今後の対策について. 臨床とウイルス. 2004. 32(1): 13-22. |
| 4. | Konno, J., Endo, K., Agatsuma, H. and Ishida, Nakao. Cyclic outbreaks of Japanese encephalitis among pigs and humans. American Journal of epidemiology. 1966. 84: 292-300. |
|
|
|
| 国立感染症研究所 感染症疫学センター/ウイルス第一部 | |
- 詳細
| 【速報一覧へ戻る】 | |
ブタの日本脳炎抗体保有状況 -2013年速報第2報-(2013年7月29日現在) |
|
| 日本脳炎は,日本脳炎ウイルスに感染したヒトのうち数百人に一人が発症すると考えられている重篤な脳炎である1)。ヒトへの感染は,日本脳炎ウイルスを媒介する蚊(日本では主にコガタアカイエカ)が日本脳炎ウイルスに感染したブタを吸血し,その後ヒトを刺すことにより起こる。 1960年代までは毎年夏から秋にかけて多数の日本脳炎患者が発生しており2),3),ブタの感染状況から日本脳炎ウイルスが蔓延している地域に多くの患者発生がみられた。当時,Konnoらは調査したブタの半数以上が日本脳炎ウイルスに感染していると,約2週間後からその地域に日本脳炎患者が発生してくると報告している4)。現在では,日本脳炎ワクチン接種の普及や生活環境の変化等により,ブタの感染状況と患者発生は必ずしも一致しておらず,近年における日本脳炎患者報告数は毎年数名程度である。しかし,ブタの抗体保有状況から日本脳炎ウイルスが蔓延あるいは活動していると推測される地域では,ヒトへの感染の危険性が高くなっていることが考えられる。 感染症流行予測調査事業では,全国各地のブタ血清中の日本脳炎ウイルスに対する抗体を赤血球凝集抑制法(HI法)により測定することで,日本脳炎ウイルスの蔓延状況および活動状況を調査している。前年の秋以降に生まれたブタが日本脳炎ウイルスに対する抗体を保有し,さらに2-メルカプトエタノール(2-ME)感受性抗体(IgM抗体)を保有している場合,そのブタは最近日本脳炎ウイルスに感染したと考えられる。下表は本年度の調査期間中におけるブタの抗体保有状況について都道府県別に示しており,日本脳炎ウイルスの最近の感染が認められた地域を青色,それに加えて調査したブタの50%以上に抗体保有が認められた地域を黄色,調査したブタの80%以上に抗体保有が認められた地域を赤色で示している。 本速報は日本脳炎ウイルスの感染に対する注意を喚起するものである。また,それぞれの居住地域における日本脳炎に関する情報にも注意し,日本脳炎ウイルスが蔓延あるいは活動していると推測される地域においては,予防接種を受けていない者,乳幼児,高齢者は蚊に刺されないようにするなど注意が必要である。 本年度の日本脳炎定期予防接種は,第1期(3回)については標準的な接種年齢である3~4歳および第1期接種が完了していない小学1~4年生(年度内に7~10歳:2003~2006年度生まれ),第2期(1回)については高校3年生相当年齢(年度内に18歳:1995年度生まれ)に積極的勧奨が行われているが,それ以外でも日本脳炎ウイルスの活動が活発な地域に居住し,接種回数が不十分な者は日本脳炎ワクチンの接種が望まれる。なお,日本脳炎の予防接種に関する情報については以下のサイトから閲覧可能である。 【 国立感染症研究所HP / 厚生労働省HP 】 |
抗体保有状況 (地図情報) 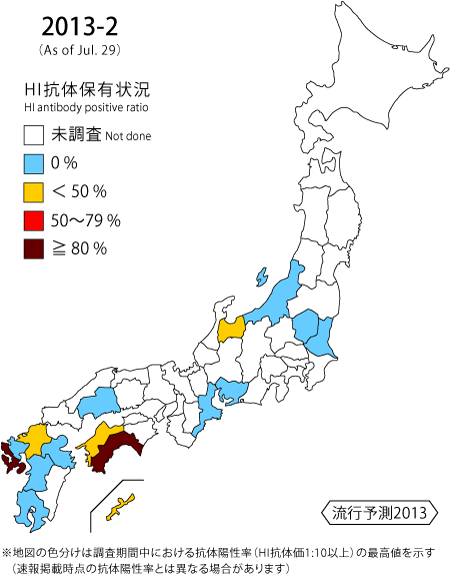 抗体保有状況 (月別推移) 
|
| HI抗体 | 2-ME 感受性 抗体 |
都道府県 | 採血 月日 |
HI抗体 陽性率 ※1 |
2-ME感受性 抗体陽性率 ※2 |
コメント |
| ◎ 5/27 |
◎ 6/24 |
沖縄県 | 7/16 | 0% (0/20) |
|
|
| |
|
鹿児島県 | 7/1 | 0% (0/20) |
|
|
| |
|
大分県 | 7/22 | 0% (0/10) |
|
|
| |
|
熊本県 | 7/23 | 0% (0/20) |
|
|
| ◎ 7/2 |
|
長崎県 | 7/23 | 100% (10/10) |
0% (0/1) |
HI抗体陽性例のうち1頭は抗体価1:40以上であったが、2-ME感受性抗体は検出されなかった。 |
| |
|
佐賀県 | 7/17 | 0% (0/10) |
|
|
| ◎ 7/23 |
◎ 7/23 |
福岡県 | 7/23 | 10% (1/10) |
100% (1/1) |
HI抗体陽性例の1頭は抗体価1:40以上であり、2-ME感受性抗体も検出された。 |
| ◎ 6/25 |
◎ 6/25 |
高知県 | 7/9 | 90% (9/10) |
50% (4/8) |
HI抗体陽性例のうち8頭は抗体価1:40以上であり、そのうち4頭から2-ME感受性抗体が検出された。 |
| ◎ 7/9 |
|
愛媛県 | 7/16 | 0% (0/10) |
|
|
| |
|
広島県 | 7/24 | 0% (0/10) |
|
|
| |
|
三重県 | 7/22 | 0% (0/20) |
|
|
| |
|
愛知県 | 7/22 | 0% (0/10) |
|
|
| ◎ 7/16 |
|
富山県 | 7/22 -23 |
10% (2/20) |
|
HI抗体陽性例はすべて抗体価1:40未満であった。 |
| |
|
新潟県 | 7/22 | 0% (0/10) |
|
|
| |
|
栃木県 | 7/16 | 0% (0/14) |
|
|
| |
|
茨城県 | 7/16 | 0% (0/10) |
|
|
| 調査期間中に調査したブタのHI抗体陽性率が80%を超えた地域 | ||||||
| 調査期間中に調査したブタのHI抗体陽性率が50%を超え,かつ2-ME感受性抗体が検出された地域 | ||||||
| 調査期間中に調査したブタから2-ME感受性抗体が検出された地域 | ||||||
| ◎ | 調査期間中に調査したブタからHI抗体あるいは2-ME感受性抗体が検出されたことを示し、日付は今シーズンで初めて検出された採血月日を示す | |||||
| ※1 HI抗体は抗体価1:10以上を陽性と判定した。 ※2 2-ME感受性抗体は抗体価1:40以上(北海道・東北地方は1:10以上)の検体について検査を行い,2-ME処理を行った血清の抗体価が未処理の血清と比較して,3管(8倍)以上低かった場合を陽性,2管(4倍)低かった場合を疑陽性,不変または1管(2倍)低かった場合を陰性と判定した。なお,2-ME未処理の抗体価が1:40(北海道・東北地方は1:10あるいは1:20も含む)で,2-ME処理後に1:10未満となった場合も陽性と判定した。 |
||||||
| 1. | Southam, C. M., Serological studies of encephalitis in Japan. II. Inapparent infection by Japanese B encephalitis virus. Journal of Infectious diseases. 1956. 99: 163-169. |
| 2. | 松永泰子,矢部貞雄,谷口清州,中山幹男,倉根一郎. 日本における近年の日本脳炎患者発生状況-厚生省伝染病流行予測調査および日本脳炎確認患者個人票(1982~1996)に基づく解析-. 感染症学雑誌. 1999. 73: 97-103. |
| 3. | 新井 智,多屋馨子,岡部信彦,高崎智彦,倉根一郎. わが国における日本脳炎の疫学と今後の対策について. 臨床とウイルス. 2004. 32(1): 13-22. |
| 4. | Konno, J., Endo, K., Agatsuma, H. and Ishida, Nakao. Cyclic outbreaks of Japanese encephalitis among pigs and humans. American Journal of epidemiology. 1966. 84: 292-300. |
|
|
|
| 国立感染症研究所 感染症疫学センター/ウイルス第一部 | |
- 詳細
(掲載日 2013/7/29)
ケニアへ渡航した8名のグループ内で、2名が熱帯熱マラリアに罹患した。1人目が診断された時点で旅行形態を把握し、注意喚起を行ったことで2人目の早期診断に至った。また同グループは黄熱ワクチンを接種したのみで、ほかのトラベラーズワクチン接種やマラリア予防内服を行っておらず、渡航者への啓発が必要な事例と考えられたため報告する。
症例1:日常生活動作は自立し、普段は畑仕事が可能な78歳女性。2013年5月29日~6月10日までケニアへ渡航した。5月30日~6月6日までニャンザ州ボンド県西アセンボ郡ランブグ村に滞在し、8日までマサイマラ、その後、ナイバシャ湖を経てナイロビに入りケニアを出国した。帰国3日目から数回転倒し、徐々に会話がかみ合わなくなり、17日に38℃台の発熱に気づかれて総合病院を受診した。受診時の意識レベルはJCS II-10 、GCS E4V5M6、血圧115/87 mmHg、脈拍 101/分、呼吸数36/分、酸素飽和濃度93%(室内気)で口腔内に点状出血、右の肋骨脊椎角叩打痛を認めた。血液検査では血小板減少、肝・腎機能障害があり、血液塗抹標本で熱帯熱マラリア原虫(原虫寄生率 3.8%)が検出された。当院へ転送される直前に血圧と酸素飽和濃度が低下し、昇圧剤と酸素投与が開始された。意識障害、循環不全、高原虫血症から重症熱帯熱マラリアと診断し、キニーネ点滴とアーテスネート座薬で治療を開始した。
症例2:アフリカへの渡航歴が複数回あり、マラリアに2回罹患して現地での治療歴がある。症例1の患者と同旅程でケニアへ渡航し行動を共にした。6月19日に38℃台の発熱、ふらつき、脱力感が出現したため当院を受診した。意識清明、身体所見では脾腫を認めた。血液検査で白血球・血小板減少、肝酵素上昇があり、血液塗抹標本で熱帯熱マラリア原虫(原虫血症0.2%)を検出し、熱帯熱マラリアと診断した。合併症はなくアトバコン・プログアニルで治療を開始した。
本事例では同じ旅程でケニアへ渡航した8名(小学生2名を含む)のうち2名が熱帯熱マラリアに罹患した。1例目が当院に入院した際の問診で、付き添いの家族から同行者がいるとの情報を得ており、同行者に発熱などの症状が出たらすぐに当院を受診するよう伝え、症例2は重症化する前に診断できたと考える。また症例2が診断された翌日、保健所を通じて同行者の健康確認を行ったところ、6月19日にもう1名が発熱し、過去に海外で購入していた抗マラリア薬を内服したとのことであった。内服終了後に当院を受診し、血液塗抹標本検査・マラリア原虫の遺伝子検査を行ったが原虫は検出されず、マラリアには罹患していなかったと思われる。食中毒の事例では、医師は同一グループ内で類症者がいないかどうかに留意し問診することが多いが、マラリアであっても患者と行動を共にした者の症状の有無を確認し、発症した場合の対処について同行者へ説明・周知することが重要と考えられる。
グループのメンバーほとんどに複数回のケニア渡航歴があり、症例2のようにマラリアの既往歴がある者もいた。マラリアの流行地に滞在するという認識はあり、防蚊対策は取っていたようである。またマラリア予防内服について若干の知識は持っていたようだが、「予防内服をすると、マラリアに感染した時に診断が遅れる」という誤った理解をしているメンバーがいた。さらにトラベラーズワクチンの接種は全員が黄熱ワクチンのみであった。最近は旅行会社から渡航先で流行している感染症、予防法などの情報提供が行われるようになった。本グループはケニア在住の知人を通じて現地旅行会社にツアーの手配を依頼しており、日本人渡航者向けに十分な情報提供がなされていなかった可能性がある。
「日本人渡航者のほとんどはトラベラーズワクチンを接種しておらず、早急な改善が必要だ」1)と批判されてから10数年、各地にトラベルクリニックが開設されトラベラーズワクチンの接種、マラリア予防薬処方や渡航先の感染症情報の提供を行っている。しかし本事例はトラベルクリニックの存在が渡航者に十分知られておらず、まだまだ活用されていない現状を物語っている。旅行医学に関わる医療者はこのような状況をふまえ、改めて一般医療機関・渡航者への啓発を行う必要があると考えられる。
参考文献
1) Basnyat B, et al., J Travel Med 7: 37, 2000
奈良県立医科大学病原体・感染防御医学/奈良県立医科大学附属病院感染症センター
中村(内山)ふくみ
奈良県立医科大学附属病院感染症センター
小川 拓 米川真輔 福盛達也 宇野健司 笠原 敬 前田光一 浦手進吾 三笠桂一
奈良県立医科大学附属病院高度救命救急センター
井上 剛 有川 翔
- 詳細
2013年7月29日
国立感染症研究所
背景
以下のリスクアセスメントは、現時点で得られている情報に基づいており、新たな情報により内容を更新していかなければならない。事態の展開にあわせてリスクアセスメントを更新していく予定である。なお、症例情報は、基本的にはWHOからの公式情報を使用してまとめた。
事例の概要
2012年9月22日に英国より中東へ渡航歴のある重症肺炎患者から後にMiddle East Respiratory Syndrome Coronavirus(MERSコロナウイルス)と命名される新種のコロナウイルス(以下、MERS)が分離されたとの報告があって以来、中東地域に居住ないし渡航歴のある者において、このウイルスによる重症呼吸器疾患の症例が継続的に報告されている。医療機関での集団発生や濃厚接触者における発症が見られ、限定的なヒト-ヒト感染が確認されている。
疫学的所見
- 2013年7月21日までに、ヒト感染の確定症例90名(死亡45名:致命率50%)が世界保健機関(WHO)に報告された。
- 中東地域からの報告症例数(死亡数)は78名(40名)であり、サウジアラビアの70名(38名)が大多数を占め、他にヨルダン、カタール、アラブ首長国連邦にて症例が見られた。
- 中東地域以外では欧州(英国、フランス、ドイツ、イタリア)および地中海沿岸部(チュニジア)にて症例が認められた。中東地域外のすべての症例は、中東地域への渡航歴のあるもの、もしくはその接触者であった。
- 感染源や感染経路は判明しておらず、調査中。発症前に動物との接触が明らかに分かっている症例はごくわずかである。
- 症例の多くは男性で(64%;性別の報告された81名中52名)、年齢は2歳から94歳(中央値50歳)であった。
- 情報が得られた範囲では、症例の多くが併存症(糖尿病、がん、慢性の心・肺・腎疾患など)を持っていた。
- 臨床症状に関して、呼吸器症状は軽症から重症なものまで多様であるが、多くの症例が入院の必要な重症肺炎を呈していた。下痢を伴うことが多く、腎不全やDICなどの合併例もあった。なお、免疫抑制状態の患者においては、初期には下痢だけを呈する可能性も指摘されている。現時点で、このウイルス感染症に特異的な治療法はない。
- 無症候の検査確定例はサウジアラビアとアラブ首長国連邦から報告あり。サウジアラビアから報告された8例のうち4例は医療従事者の女性、他の4例は確定例との接触歴のある小児(7~15歳)であった。アラブ首長国連邦は2名の医療従事者。
- 2012年4月にヨルダンの医療機関で集団発生事例が発生していたことも明らかになっている(確定症例2名と疑い症例11名、うち10名は医療従事者)。
※ 学術論文から得られた疫学情報
- 2013年4月1日から5月23日の間に、サウジアラビアの東部地域において23例の確定例(それ以外に11例の可能性例も存在)の報告があったが、これは4つの医療施設が関与したアウトブレイクであった。確定例23例のうち21例が、透析室、集中治療室、入院病棟においておこり、その中にはヒト—ヒト感染が確認された例もあったが、その感染様式は特定することができなかった。200名以上の医療従事者が接触者として経過観察がなされ、確定症例の治療に携わった医師と、確定症例との接触が明らかでなかった管理職看護師の計2名が確定診断された。一方217名の家族が経過観察され、うち3名が確定診断された。潜伏期間は中央値5.2日(95%信頼区間:1.9-14.7日)、世代間隔(感染源の発症から二次感染者の発症までの期間)は、中央値7.6日(95%信頼区間:2.5-23.1日)と推定されている。なお、分離ウイルス4株の遺伝子解析では、単一のクレードであることが示された[1]。
- イギリスにおいて2013年2月に発生した二次感染者2名の家族集積例における潜伏期間は1-9日と推定されている[2]。
- サウジアラビアで2012年10-11月に発生した家族内集積事例の報告では、同居家族のうち男性のみに感染伝播が起こり(確定例2名、可能性例1名)、入院前のみに濃厚接触があったこれらの症例の配偶者は感染していないことから、病初期においては感染性が低い可能性が推察されている[3]。
- フランスではドバイから帰国して発症した1例とこの患者から院内感染した1例の計2例が報告された。本事例では、ウイルス検出のためには下気道からの検体が必要であることが指摘され、また潜伏期間は9-12日と推定されている[4]。
- 6月21日までの64症例から計算された基本再生産数(R0)は、低めの推計値(集団発生内に複数の初感染例を仮定)で0.60 (95% CI 0.42–0.80)、高めの推計値(集団発生ごとに一つの初感染例を仮定)で0.69 (0.50–0.92)といずれも1.00を下回った。2003年のSARSのR0が0.80 (0.54–1.13)であり、MERSのR0はこれより低く、パンデミックは起こしがたいと推察されている[5]。
ウイルス学的所見
英国(n=2)、サウジアラビア(n=1)、ヨルダン(n=1)、ドイツ(n=1)の患者検体から計5株のウイルスが分離され、それらの遺伝子の塩基配列が公開されている。これらの株間では99%以上の遺伝子塩基配列の相同性がみられた。最近の報告ではMERSと非常に近いコロナウイルスがSouth Africa batから分離されている[6]。
WHOによる対応
- 症例定義の発出(7月3日改訂)。
http://www.who.int/csr/disease/coronavirus_infections/case_definition/en/index.html - サーベイランスガイダンスの発出(6月27日改訂)。
http://www.who.int/csr/disease/coronavirus_infections/InterimRevisedSurveillanceRecommendations_nCoVinfection_27Jun13.pdf
6月27日に発出された改訂されたサーベイランスガイダンスでは、診断のためには、下気道からの検体採取が勧められること、また潜伏期については多くの事例は1週間未満であると考えられるが、潜伏期が9-12日という事例があるため、確定例の接触者や中東への渡航歴があるものについては、14日間の健康観察が勧められている。 - 症例調査ガイダンスの発出。
http://www.who.int/csr/disease/coronavirus_infections/MERS_CoV_investigation_guideline_Jul13.pdf - 診断プロトコールの発出。
http://www.who.int/csr/disease/coronavirus_infections/LaboratoryTestingNovelCoronavirus_21Dec12.pdf - バイオリスクマネジメントのガイダンスの発出。
http://www.who.int/csr/disease/coronavirus_infections/Biosafety_InterimRecommendations_NovelCoronavirus_19Feb13.pdf - 医療機関における、感染予防・コントロールのガイダンスの発出。
http://www.who.int/csr/disease/coronavirus_infections/IPCnCoVguidance_06May13.pdf - 治療に関するガイダンスの発出。
http://www.who.int/csr/disease/coronavirus_infections/InterimGuidance_ClinicalManagement_NovelCoronavirus_11Feb13u.pdf - 症例対象研究に関するプロトコールの作成と共有(7月3日改訂)。
http://www.who.int/csr/disease/coronavirus_infections/MERSCoVCaseControlStudyPotentialRiskFactors_03Jul13.pdf - 国際重症急性呼吸器・新興感染症協会(International Severe Acute Respiratory and Emerging Infection Consortium)とともに、病因・薬理学的研究のための研究プロトコール・症例報告様式の作成と共有。
http://www.prognosis.org/isaric/ - 国際保健規則(IHR)に基づく対応:緊急委員会の開催(第一回7月9日、第二回7月17日)
現時点では「国際的に懸念される公衆の保健上の緊急事態(PHEIC)」には至っていないが、継続した監視、感染防止策、渡航に関する勧告、リスクコミュニケーション、研究、IHRに基づく通告の徹底が重要であると確認。 - サウジアラビアへの巡礼者向けの暫定的な渡航時の助言(7月25日発出)
WHOは入国時の特別なスクリーニングおよび渡航や貿易を制限することを推奨しない。各国に対し、巡礼者のみならず、輸送業者、地上職員など巡礼者の渡航に関連する人でのMERS感染のリスクを軽減するために、渡航時の助言や渡航者の自己申告に関する認識を向上するよう奨励する。
http://www.who.int/ith/updates/20130725/en/index.html
国内対応
- 感染研ウイルス第三部より検査試薬(PCR用プライマー・プローブ、陽性対照等)が各地方衛生研究所および政令指定都市の保健所計72箇所に配布された。
- 2012年9月26日付で、MERS感染症が疑われる事例について厚生労働省への情報提供をするようにとの通知が出されている。その後2012年11月30日付で症例定義が、発症前10日以内にアラビア半島またはその周辺国に渡航または居住していた者と変更されている。2013年5月24日には、MERSによる感染症疑い患者が発生した場合の標準的対応フローが厚生労働省から自治体等に向けて発出された。
- l感染研はWHO等からの情報の翻訳をし、ウェブサイトを通じて情報提供している。
リスクアセスメントと今後の対応
- 現時点で、医療機関内や家族間などにおいて、限定的なウイルス伝播が確認されている。医療従事者における感染事例が確認されているが、感染様式については明らかになっていない。
- いずれの事例においても感染が市中へ急速に拡大しているという疫学的所見はなく、人-人感染は限定的と考えられている。
- 一部のクラスターを除くと、中東の比較的広い地域において散発的に患者が発生しているが、その感染源は依然として不明である。コロナウイルスの特性から、自然宿主とは別にヒトに感染を起こしている中間宿主が存在する可能性が指摘されている。
- 報告された症例のうち多くが死亡の転帰をとっているが、新たな感染症が出現した際には最も重症な症例から発見される傾向にあり、不顕性感染者や軽症例がつかめていない可能性がある、当該疾病の真の病態像や重症度といった全体像については、十分な検討が行えていない。
- 昨年9月に本疾患が初めて報告されて以来、世界各国においてサーベイランスが強化されてきたところであるが、現時点では、中東外ではヨーロッパとチュニジアにおいて帰国者(輸入例)とその接触者感染が少数確認されているのみである。
- 日本においても、今後、中東からの輸入例が探知される可能性はありうると考え、関係機関は海外での発生状況などの情報に注意し、国内において輸入例が発見された際には院内感染対策等に細心の注意を払う必要がある。
参考文献
- Assiri A, McGeer A, Perl TM, Price CS, Al Rabeeah AA, Cummings DA, Alabdullatif ZN, Assad M, Almulhim A, Makhdoom H, Madani H, Alhakeem R, Al-Tawfiq JA, Cotten M, Watson SJ, Kellam P, Zumla AI, Memish ZA; the KSA MERS-CoV Investigation Team. Hospital Outbreak of Middle East Respiratory Syndrome Coronavirus. N Engl J Med. 2013 Jun 19. [Epub ahead of print]
- Health Protection Agency (HPA) UK Novel Coronavirus Investigation team. Evidence of person-to-person transmission within a family cluster of novel coronavirus infections, United Kingdom, February 2013. Euro Surveill. 2013 Mar 14;18(11):20427.
- Memish ZA, Zumla AI, Al-Hakeem RF, Al-Rabeeah AA, Stephens GM. Family cluster of Middle East respiratory syndrome coronavirus infections. N Engl J Med. 2013 Jun 27;368 (26):2487-94.
- Guery B, Poissy J, El Mansouf L, Séjourné C, Ettahar N, Lemaire X, Vuotto F, Goffard A, Behillil S, Enouf V, Caro V, Mailles A, Che D, Manuguerra JC, Mathieu D, Fontanet A, van der Werf S; the MERS-CoV study group. Clinical features and viral diagnosis of two cases of infection with Middle East Respiratory Syndrome coronavirus: a report of nosocomial transmission. Lancet. 2013 Jun 29;381 (9885):2265-72
- Breban R, Riou J, Fontanet A. Interhuman transmissibility of Middle East respiratory syndrome coronavirus: estimation of pandemic risk. doi:10.1016/S0140-6736(08)61345-8
- Ithete NL, Stoffberg S, Corman VM, Veronika M. Cottontail VM, Richards LR, Schoeman MC, Drosten C, Drexler JF, Preiser W. Close Relative of Human Middle East Respiratory Syndrome Coronavirus in Bat, Emerg Infect Dis . 2013 Oct 19(No.10)