お知らせ
感染症情報
研究・検査・病原体管理
サーベイランス
刊行・マニュアル・基準
- 詳細
エンテロウイルス無菌性髄膜炎由来ウイルス週別都道府県別 |
- 詳細
インフルエンザウイルス都道府県別都道府県別・週別
週別
|
- 詳細
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
〈第23週コメント〉 6月13日集計分 ◆全数報告の感染症 注意:これは当該週に診断された報告症例の集計です。しかし、迅速に情報還元するために期日を決めて集計を行いますので、当該週に診断された症例の報告が集計の期日以降に届くこともあります。それらについては一部を除いて発生動向総覧では扱いませんが、翌週あるいはそれ以降に、巻末の表の累積数に加えられることになります。 *感染経路、感染原因、感染地域については、確定あるいは推定として記載されていたものを示します。
全国の指定された医療機関(定点)から報告され、疾患により小児科定点(約3,000 カ所)、インフルエンザ(小児科・内科)定点(約5,000 カ所)、眼科定点(約600 カ所)、基幹定点(約500 カ所)に分かれています。また、定点当たり報告数は、報告数/定点医療機関数です。
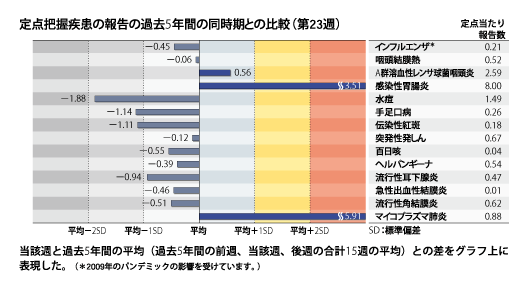
インフルエンザ:定点当たり報告数は第6週以降減少が続いている。都道府県別では沖縄県(5.67)、熊本県(1.34)、宮崎県(0.97)、鹿児島県(0.95)が多い。 小児科定点報告疾患:RSウイルス感染症の報告数は325例と2週連続で減少した。年齢別では1歳以下の報告数が全体の約77%を占めている。咽頭結膜熱の定点当たり報告数は3週連続で増加した。都道府県別では宮崎県(1.19)、佐賀県(1.13)、福岡県(0.92)、福井県(0.91)が多い。A群溶血性レンサ球菌咽頭炎の定点当たり報告数は減少した。都道府県別では宮崎県(4.72)、大分県(4.39)、山形県(4.27)が多い。感染性胃腸炎の定点当たり報告数は2週連続で減少したが、過去5年間の同時期(前週、当該週、後週)と比較してかなり多い。都道府県別では香川県(13.6)、福井県(12.9)、山形県(12.3)、兵庫県(11.6)が多い。水痘の定点当たり報告数は増加した。都道府県別では長野県(2.57)、山形県(2.13)、埼玉県(2.02)が多い。手足口病の定点当たり報告数は第19週以降増加が続いている。都道府県別では青森県(1.76)、福井県(1.55)、新潟県(1.23)が多い。伝染性紅斑の定点当たり報告数は2週連続で増加した。都道府県別では高知県(0.87)、山形県(0.83)、鳥取県(0.74)が多い。百日咳の定点当たり報告数は減少した。都道府県別では高知県(0.50)、岩手県(0.30)、新潟県(0.15)、広島県(0.15)が多い。ヘルパンギーナの定点当たり報告数は第19週以降増加が続いている。都道府県別では三重県(3.31)、宮崎県(2.42)、熊本県(1.90)が多い。流行性耳下腺炎の定点当たり報告数は減少した。都道府県別では岩手県(1.85)、大分県(1.06)、山形県(0.93)が多い。 基幹定点報告疾患:マイコプラズマ肺炎の定点当たり報告数は増加し、過去5年間の同時期と比較してかなり多い。都道府県別では栃木県(3.00)、福島県(2.86)、富山県(2.60)が多い。 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
- 詳細
2012年第23週(第23号)
(6月4日~6月10日)発生動向総覧 /注目すべき感染症(腸管出血性大腸菌感染症)/病原体情報(麻疹ウイルス2012年)/速報(A群ロタウイルスによる胃腸炎集団事例発生状況-千葉県) 〔2012年6月22日発行〕
- 詳細
生のヒラメを原因としたKudoa septempunctata による食中毒事例-奈良市
(IASR Vol. 33 p. 152-153: 2012年6月号)
本事例は、奈良県内において生のヒラメを原因とするKudoa septempunctata (以下、クドア)による食中毒として断定した初めての事例であり、疫学調査と検査成績から一定の知見を得たので報告する。
概 要
2011(平成23)年10月3日に原因施設から連絡を受け食中毒調査を開始した。その結果、当該施設が10月1日の昼食として調製した弁当等を喫食した2組20名のうち14名が、10月1日14時を初発として嘔気、嘔吐、発熱、下痢等の症状を呈したことがわかった。また、原因施設に保管されていたヒラメの切り身(患者らに造り等として提供したヒラメと同一個体のもの。以下同じ)および喫食残品の生のヒラメからクドア胞子を検出し、患者4名の糞便からクドアの18S rRNA遺伝子を検出した。
発症状況
患者14名は嘔気、嘔吐、発熱、下痢を主症状とし、当該食事を起点とした潜伏期間は3~7.5時間(中央値5.5時間)と短いのが特徴であった(表1、表2)。主な初期症状は、嘔気、嘔吐、腹痛であり、続いて下痢、発熱の症状を呈した。嘔吐および下痢の症状の平均持続時間は、それぞれ 3.4時間、 6.1時間と短く、比較的軽症であった(表2)。
検査方法
クドアの検査については、大阪府立公衆衛生研究所および国立医薬品食品衛生研究所に依頼した。食品検体(ヒラメ、マグロ、カンパチ、サーモン)のうち、ヒラメについては大阪府立公衆衛生研究所により顕微鏡検査と遺伝子検査を実施し、マグロ、カンパチ、サーモンについては国立医薬品食品衛生研究所により顕微鏡検査を実施した。また、患者糞便検体については大阪府立公衆衛生研究所により遺伝子検査を実施した。なお、遺伝子検査は大阪府立公衆衛生研究所により報告された方法1) を用いた。
検査結果
原因施設に保管されていたヒラメの切り身および喫食残品の生のヒラメからクドア胞子(1.1×107個/g)およびその18S rRNA遺伝子が検出された。一方、ヒラメ以外の生のマグロ、カンパチおよびサーモンでは、クドア胞子は検出されなかった(表3)。患者9名のうち4名の糞便からクドアの18S rRNA遺伝子が検出され、そのCycle threshold (Ct)値は36.26~40.69であった。また、クドアを検出した患者4名における当該食事の喫食から糞便検体採取までの期間は、2.5~3.9日(中央値3日)であった。
ヒラメの喫食状況およびクドア胞子の摂取量
患者1名当たり少なくとも15~16g以上のヒラメの喫食が認められた。この喫食量からクドア胞子の摂取量を概算すると、患者1名当たり摂取胞子数は1.7×108個~5.8×108個(中央値1.7×108個)であった。この結果は、2010(平成22)年10月に発生した特定の養殖ヒラメの喫食を原因とする食中毒事例より推定されたクドア胞子の最少摂取量(7.2×107個)2) を上回るものであった。
ヒラメの販売系統の調査
汚染経路の追及としてヒラメの販売系統の調査をした結果、患者らに提供のあったのは輸入された養殖ヒラメであることを確認した。なお、養殖業者および養殖場については特定できなかった。
考 察
本事例は、患者の喫食状況と発症状況からクドアによる食中毒が疑われ、生のヒラメと患者糞便からクドア胞子あるいはクドア遺伝子が検出されたこと、また、他の食中毒菌等の検査結果から病因物質を特定できる状況はなかったことから、クドアを病因物質とする食中毒と断定した。生のヒラメによる食中毒は、クドアの関与が強く示唆されているものの、発症機序、症状の発現状況および最小発症量等のデータが十分ではないことから、クドアを病因物質として特定するにあたって他の食中毒菌等の検査結果を考慮する必要がある。このような状況のもと、クドアの糞便の検査を実施したことによって病因物質の早急な特定につながったことは、食品衛生上の危害の拡大を防止するうえで非常に有益であった。また、クドアの予防策として養殖段階における保有稚魚の排除等の対応を検討するにあたって、輸入者等はロットごとにヒラメの養殖場を特定できる生産履歴等の書類を保管し、流通の各段階では、異なる養殖場のヒラメを混同しないよう管理していくことが重要であると考えた。
謝辞:本事例に関して、クドアの検査にご協力いただいた大阪府立公衆衛生研究所および国立医薬品食品衛生研究所の各位に深謝いたします。
参考文献
1) Harada T, et al ., Int J Food Microbiol 156: 161-167, 2012
2)薬事・食品衛生審議会食品衛生分科会食中毒・乳肉水産食品合同部会資料2(平成23年4月25日開催)
奈良市保健所
安宅弘充 小泉拓也 中川昌子 田中敬大 藤橋和生 菅 雪恵 山口武彦 河辺隆雄 松本善孝
- 詳細
クドア食中毒総論
(IASR Vol. 33 p. 149-150: 2012年6月号)
2008(平成20)年後半から、国立医薬品食品衛生研究所を中心に国立感染症研究所、大学、各自治体および地方衛生研究所が協力して解明に取り組んできた生鮮魚介類の生食を原因とする原因不明食中毒は、2011(平成23)年6月に厚生労働省により、その病因物質は、ヒラメに寄生するKudoa septempunctata (和名:ナナホシクドア)である可能性が非常に高いとの結論を得た。本食中毒はクドア属寄生虫による世界初の食中毒であることからクドア食中毒と呼ぶ。
クドア食中毒は、検査法が通知された平成23年6~12月までに計33件が報告されている(表1)。発生に季節性が観察されており、9、10月に多発するという特徴をもつ。クドア食中毒原因の大部分は養殖ヒラメが占めているが、養殖ヒラメは韓国産および国産が消費量のほとんどを占める(平成23年統計)。ヒラメの消費量は12月および1月が最も多く、当該食中毒の発生頻度と消費量との相関は認められない。
2009(平成21)年10月に愛媛県で起こったヒラメ喫食を原因とする食中毒事例では100名以上の患者を出し、その食中毒の疫学的特徴が明らかになった。調査結果によると、症状は下痢が79.7%で最も多く、次いで嘔吐(57.6%)の順であり、潜伏期の中央値は5.0時間(範囲:1.0~22.0時間)であった。多くの場合24時間以内に症状は治まり、予後は良好であり、後遺症の報告はなかった。この事例から推定される発症摂取胞子数は7.2×107個であった。今後報告される事例から、より詳細な発症摂取胞子数を推定し、検査法等に取り入れていく必要がある。
K. septempunctata はミクソゾア門という生物群に属す粘液胞子虫類の一種である。粘液胞子虫類は世界中で2,000種以上報告されており、近年の分子系統学的解析から、クラゲやイソギンチャクなどの刺胞動物の近縁であることが明らかになっている。そのほとんどが魚類の寄生虫である。クドア属粘液胞子虫は、形態学的には内部にコイル状の極糸を持つ極嚢という構造がある胞子を形成する多細胞動物で、極嚢と胞子原形質を包含する胞子殻から成る。K. septempunctata は、約10μmの大きさを呈し、極嚢の数が5~7個である。今までに報告されている筋肉寄生クドアは、ブリの奄美クドア症原因種であるK. amamiensis やサケなどに寄生するK. thyrsites がその代表としてあげられる。シストが肉眼的に確認できたり、ジェリーミートを呈したりすることで商品価値を落とすことから水産業界では問題とされているが、食中毒の報告はない。一方、本食中毒の病因物質であるK. septempunctata は、シストも形成しなければジェリーミートにもならないため、調理の過程でその存在を見過ごしてしまう大きな原因となっている。
K. septempunctata の生活環はまだ解明されていないが、すでに解明されている淡水種の魚に寄生するクドア属の例では、魚類と環形動物を交互に宿主とする。魚体内から粘液胞子虫の胞子が体外に放出されると、環形動物(淡水種ではイトミミズなどの貧毛類)に食べられ、その腸管内で胞子は胞子原形質を出し腸管上皮から侵入する。環形動物の腸管細胞内で有性生殖が行われ、形態の全く異なる放線胞子虫に変態し水中に放出する。放線胞子虫は先端に原形質を有し3本の突起により浮遊している間に魚と接触すると、皮膚感染により魚体内に原形質が侵入し、粘液胞子虫のステージが始まると考えられている。このような生活環を考慮すると、魚から魚への水平感染は一般に起こらない。すなわち養殖場の水槽内や飲食店のイケス内で粘液胞子虫が感染することはないと考えられる。K. septempunctata は、生きた状態でヒトに喫食されないと食中毒は起こらないことがわかっている。また、従来の寄生虫性食中毒と異なり、腸管や生体内での増殖は認められていない。
毒性研究において、クドア食中毒の下痢原性は乳飲みマウスおよびヒト腸管培養細胞によって証明されている。メカニズムとしては、腸管に至った生きたクドア胞子から胞子原形質が出て、腸管に進入する可能性が推測されている。嘔吐毒性はスンクスにおいて証明されているが、メカニズムは不明である。
国立医薬品食品衛生研究所衛生微生物部 小西良子