鳥インフルエンザA(H7N9)ウイルスによる感染事例に関するリスクアセスメントと対応
平成29年8月31日現在
国立感染症研究所
背景
今回、中国における鳥インフルエンザA(H7N9)ウイルス感染症の第5波(2016年10月1日以降)におけるヒトの報告数がピークを越えて減少傾向に転じたこと、及び高病原性鳥インフルエンザA(H7N9)ウイルスに感染した患者数の報告を受けて、リスクアセスメントをアップデートする。今後も、事態の展開があれば、リスクアセスメントを更新していく予定である![]() 。
。
疫学的所見
1)事例の概要
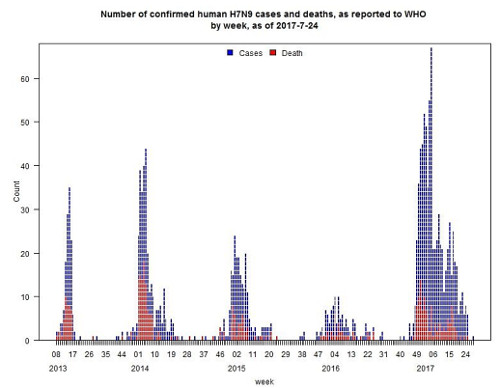
- 最初の鳥インフルエンザA(H7N9)ウイルス(以下、H7N9ウイルス)に感染した患者は、2013年3月に中国からWHOへ報告された。以後、2017年7月25日現在までに、中国本土からの報告例、もしくは中国本土に滞在歴があるか、中国本土から輸入した家禽との接触歴のある台湾・香港・マカオ・マレーシア・カナダからの患者を含め、1557例が報告されており、うち少なくとも605例(39%)が死亡している。患者の発生は、中国での冬季にピークを示し、2013年から現在までで5つのピークを認めている。第5波(2016年10月1日~)は、第1~4波に比較し、感染者数、地理的広がり共に規模が大きかったが減少傾向となっている1(図1参照)。
- 中国からWHOに報告されたデータによると、第1波の患者数は135例、第2波は320例、第3波は226例、第4波は119例と報告されている2。また、第5波については、ECDCのみ具体的な人数を公開しており、2017年7月13日の時点で、758例(2016年疫学週第41週~)と報告されている3。
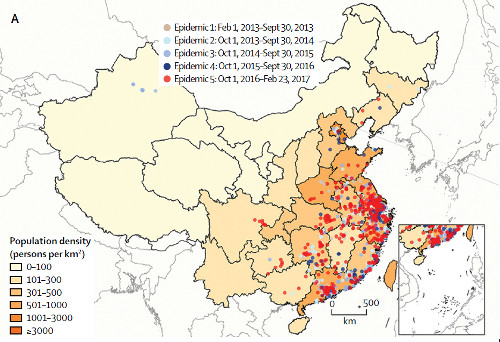
- 中国の研究グループによる、2013年2月~2017年2月に報告された1220例の確定例の解析によると、第4波や第5波では、第1~3波に比べ準市街地や農村地域からの報告が多かった4。また、年齢分布では、第1波では、60歳以上の報告の割合が多かったが、第5波では16~59歳の割合が増加していることが分かった。しかし、性別、家禽への曝露歴の有無、入院患者の重症度、については、これまでの流行期と変わっていないことが報告された。本研究による中国本土からの報告の分布を示す(図2参照)。
- 第1波から第4波では、計26のクラスター(少なくとも2例以上のリンクのある患者)を認めた(うち3は院内感染、残りは家族内での発生)5。第5波では、これまでに7つの省または市、自治区(安徽省、江蘇省、河北省、浙江省、陝西省、チベット、北京市)から計10のクラスターを認めている6,7-11。このうち4つのクラスターでは家庭内での接触による感染が疑われているが、生鳥への接触歴を認めているため8-11、鳥への共通曝露も否定できない。これまでに、3次感染例は認めていない。
- Chinese National Influenza Centerによると、2017年8月14日の時点で、広東省、湖南省、広西チワン族自治区、台湾(広東省への旅行歴あり)から計25例の高病原性H7N9ウイルス感染症 (HPAI)の患者が報告されている12。
- 2016年9月1日~2017年3月31日の期間に広東省(2例)、湖南省(1例)、広西チワン族自治区(5例)で検出された8例と中国全土から検出された低病原性H7N9感染症(LPAI)553例を比較した研究によると、HPAIの方が、田舎に在住、病鳥・死鳥との接触歴があり、また、発症から入院までの期間が短い傾向にあった13。また、2016年11月1日~2017年3月31日の期間に広東省で検出されたHPAIの9例とLPAI 感染症の51例を比較した研究によると、入院期間はHPAIで長い傾向にあったが、臨床症状や転帰に差は認めなかった。また、病気或いは死んだ鳥への接触が最大のリスク因子であると考察されている14。
2)臨床情報
-
これまでの報告から、潜伏期間は多くが3日~7日(最長10日)と推定されている15。
- 発熱、咳嗽、呼吸困難、頭痛、筋肉痛、全身倦怠感などの症状が出現し、患者の多くは、重症肺炎の病像を呈する16。一方で、軽症から中等度の病像を呈し、インフルエンザ様疾患に対する病院定点サーベイランスで探知された報告もある17。
- 死亡10例と生存30例を比較した疫学研究によると、死亡のリスク因子として高齢、慢性肺疾患、免疫不全状態、長期の投薬歴、オセルタミビル投与の遅延(生存例で発症から治療までの中央値で4.6日、死亡例で7.4日。両群ともオセルタミビル感受性あり)が報告されている18。
- H7N9ウイルス感染症に関して、リアルタイムRT-PCR法による呼吸器検体を用いた検査が推奨されている19。
3)感染源・感染経路
- 調査が可能であった第5波(2016年9月~同年12月)の97例中、87例(90%)では、鳥への接触歴があり、そのうち72例(83%)が生鳥市場への訪問歴があった。対応として、広東省、浙江省では都市部での生鳥の取引を禁止し、食鳥処理場は集約化されている。また、江蘇省や安徽省などの多くの患者が報告されている地域でも生鳥市場を禁止するなどの対応がとられている6。
- 広東省から報告されたHPAI 2例と台湾から報告されたHPAI 1例からノイラミニダーゼ阻害剤に対して低感受性を示すウイルス遺伝子変異が検出されている20。いずれの患者でも検体採取前に抗ウイルス薬が投与されており、二次感染は発生していない。また、全ての患者が治療抵抗性であったわけではなかった。
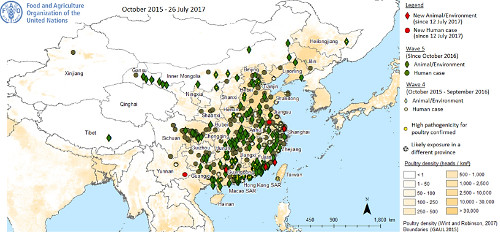
- 第5波で、ヒト感染例の報告が急増した原因の一つとして、生鳥市場や生鳥に関連する環境からのサンプル中のH7N9ウイルス陽性率の増加が2016年の12月に認められ、以前の流行より相対的に早かったことが示唆されている13。患者が多く報告されている地域では、飼育鳥に関連する環境中のウイルス検出数が多く報告されている(図3参照)。2017年2月22日から28日に広東省の9都市27か所の市場で行われたサンプリング調査において、855検体が採取され、83検体(10%)がH7陽性であった21。なお,これまでに、中国本土の野鳥からもH7N9ウイルスが検出されたことが報告されている22。
ウイルス学的所見
2013年に中国で初めてヒト感染事例を引き起こしたH7N9ウイルスは少なくとも3種類の異なる鳥インフルエンザウイルスの遺伝子再集合体であると考えられ、家禽に対して低病原性を示し、ヒトに感染すると重篤な症状を来し得ることが報告されている。第4波までに分離されたウイルスは全て家禽に対して病原性が低い低病原性ウイルスであったが、第5波では患者および生鳥市場の鶏や環境から家禽に対して高い病原性を示唆する変異を有したウイルス(高病原性ウイルス)が分離されている。高病原性ウイルス変異株も含め、H7N9ウイルスは、継続的にヒト-ヒト間で感染伝播するような能力は獲得していない13,23-25。これまでのところ、高病原性ウイルスの出現でヒトに対する疫学的パターンに変化がみられた証拠はなく、低病原性ウイルスから高病原性ウイルスへの変異により、ヒトでの病原性や感染力に影響を及ぼすという科学的な根拠は認められていない26。これまでに分離された低病原性ウイルスの主な遺伝子解析所見については、2014年のリスクアセスメントに記載している。
米国CDCの報告によると、GISAIDに登録された第5波のヒト感染例および生鳥市場環境から集められた74株のH7N9ウイルスのHA遺伝子の塩基配列解析から、遺伝子系統樹では大きく2つのクラスターに分かれ(Pearl River Delta群とYangtze River Delta群)、そのうち93%(69株)はYangtze River Delta群に属することを明らかにしている2。
WHOインフルエンザ協力センター(米国CDC, 米国St Jude小児研究病院)で実施された抗原解析の結果、Pearl River Delta群に属するウイルスはWHOが推奨する2013年のワクチン候補ウイルスと抗原的に類似しているが、流行の主流となっているYangtze River Delta群に属するウイルスはワクチン候補ウイルスから抗原性が変化しており、この群から新たに2株のワクチン候補株(A/Guangdong/17SF003/2016-like virus, A/Human/2650/2016-like virus)が作製されることになった27。
日本国内の対応
2013年4月26日、「鳥インフルエンザ(H7N9)を指定感染症として定める等の政令」(2013年政令第129号)、「感染症の予防及び感染症の患者に対する医療に関する法律施行令の一部を改正する政令」(2013年政令第130号)、「検疫法施行令の一部を改正する政令」(2013年政令第131号)等が公布され、鳥インフルエンザA(H7N9)は指定感染症に定められた。それに伴い、2013年5月2日付の厚生労働省通知により、38℃以上の発熱及び急性呼吸器症状があり、症状や所見、渡航歴、接触歴等から鳥インフルエンザA(H7N9)が疑われると判断した場合、保健所への情報提供を行い、保健所との相談の上、検体採取(喀痰、咽頭拭い液等)を行うこととなった。2015年1月21日、「感染症の予防及び感染症の患者に対する医療に関する法律第 12 条第1項及び第 14 条第2項に基づく届出の基準等について」(2006 年3月8日健感発第0308001 号厚生労働省健康局結核感染症課長通知)の別紙「医師及び指定届出機関の管理者が都道府県知事に届け出る基準」の一部が改正され、鳥インフルエンザA(H7N9)を指定感染症として定める等の政令が廃止された。現在、鳥インフルエンザA(H7N9)は二類感染症に定められている。二類感染症に追加後の対応に関しては、鳥インフルエンザA(H7N9)に感染した疑いのある患者が発生した場合における標準的な対応において変更はない。
リスクアセスメントと今後の対応
- 夏季に入り、中国のH7N9ウイルス感染症の患者報告数は減少傾向にあるため、日本国内への患者の流入の可能性も冬季に比べると低くなると考えられる。しかし、H7N9ウイルスの発生地域へ渡航する際には、生鳥市場への訪問や病鳥との接触を控えるなどの注意喚起は継続すべきである。
- 発生地域において鳥との接触があり、渡航後に発熱を認めるなどの体調の変化があった場合には、医療機関の受診時に渡航歴を伝えることの啓発が必要である。
- 限定的なヒト-ヒト感染があることから、国内に入国した感染者から家族内などで二次感染が起こりうる。
- しかしながら、先に記した疫学的・ウイルス学的所見から、ヒトへの感染が確認されているH7N9ウイルスは、ヒト-ヒト間で容易に感染伝播するような能力は獲得しておらず、持続的なヒト-ヒト感染の可能性は低いと考えられる。
- 第5波では高病原性H7N9ウイルスが生鳥市場の環境や家禽から分離され、このウイルスに罹患した患者も報告されているが、現時点ではヒトにおいて病原性が異なることを示唆する科学的根拠は明らかではない。また、これらの高病原性H7N9ウイルスによるヒト感染例ではノイラミニダーゼ阻害剤に対し低感受性を示すウイルス遺伝子変異が検出されたが、この抗ウイルス剤耐性は当該患者に対するノイラミニダーゼ阻害剤の前投与により誘導された可能性が考えられる。
- 抗原性の変化しているウイルス群が増えていること、その群に高病原性H7N9ウイルスが属していることを踏まえ、WHOは新たに2株のH7N9ワクチン候補ウイルス株を推奨した。
- 感染研は 「鳥インフルエンザA(H7N9)ウイルス感染症に関する臨床情報のまとめ:臨床像・検査診断・治療・予防投薬」を2013年4月26日に、「鳥インフルエンザA(H7N9)ウイルス感染症に対する院内感染対策」を2013年5月17日に、「鳥インフルエンザA(H7N9) 患者搬送における感染対策」を2014年7月16日に、感染研ホームページに掲載しているところであるが、今後もWHO、中国等からの情報に基づき、正確な情報を提供していく。
参考文献
- World Health Organization. Influenza at the human-animal interface. Summary and assessment, 16 June to 25 July 2017
- Iuliano AD, Jang Y, Jones J, et al. Increase in Human Infections with Avian Influenza A(H7N9) Virus During the Fifth Epidemic — China, October 2016–February 2017. MMWR. 2017;66(9):254–255.
- ECDC. Communicable Disease Threats Report, 22 July 20174. Wang X, Jiang H, Wu P, et al. Epidemiology of avian influenza A H7N9 virus in human beings across five epidemics in mainland China. 2013–17: an epidemiological study of laboratory-confirmed case series. Lancet infect Dis 2017; 17(8):822-832.
- Lei Zhou, Ruiqi Ren, Lei Yang, et al. Sudden increase in human infection with avian in uenza A(H7N9) virus in China, September–December 2016. WPSAR 2017; doi: 10.5365/wpsar.2017.8.1.001
- Xiang N, Li X, Ren R, et al. Assessing Change in Avian Influenza A(H7N9) Virus Infections During the Fourth Epidemic-China, September 2015-August 2016. MMWR. 2016; 65(49): 1390-1394.
-
Zhou L, Ren R, Yang L, et al. Sudden increase in human infection with avian influenza A(H7N9) virus in China, September–December 2016. Western Pac Surveill Response J. 2017;18;8(1):6-14.
- World Health Organization. Disease outbreak news, 15 March 2017virus in China. N Engl J Med 2014; 370:520.
- World Health Organization. Disease outbreak news, 18 April 2017A(H7N9) infection in China. Clin Infect Dis 2013; 57:1506.
- World Health Organization. Disease outbreak news, 20 April 2017
- World Health Organization. Disease outbreak news, 23 May 2017
- World Health Organization. Disease outbreak news, 28 June 2017.
- Chinese National Influenza Center. Chinese Influenza Weekly Report.
- Zhou L, Tan Y, Kang M, et al. Preliminary Epidemiology of Human Infections with Highly Pathogenic Avian Influenza A(H7N9)Virus, China, 2017. Emerg Infect Dis. 2017;23(8):1355-1359.
- Kang M, Lau EHY, Guan W, et al. Epidemiology of human infections with highly pathogenic avian influenza A(H7N9) virus in Guangdong, 2016 to 2017. Euro Surveill. 2017;6;22(27).
- Li Q, Zhou L, Zhou M, et al. Epidemiology of human infections with avian influenza A (H7N9) virus in China. N Engl J Med. 2014;370:520.
- Ke Y, Wang Y, Liu S, et al. High severity and fatality of human infections with avian influenza A(H7N9) infection in China. Clin Infect Dis. 2013;57:1506.
- Ip DK, Liao Q, Wu P, et al. Detection of mild to moderate influenza A/H7N9 infection by China’s national sentinel surveillance system for influenza-like illness: case series. BMJ. 2013;346:f3693.
- Liu S, Sun J, Cai J, et al. Epidemiological, clinical and viral characteristics of fatal cases of human avian influenza A(H7N9) virus in Zhejiang Province, China. J Infect. 2013;67(6):595-605.
- Interim Guidance for Specimen Collection, Processing, and Testing for Patients with Suspected Infection with Novel Influenza A Viruses Associated with Severe Disease in Humans.
- World Health Organization. Disease outbreak news, 27 February 2017
- Food and Agriculture Organization of the United Nations (FAO). H7N9 situation update, 26 July 2017.
- Zhao B, Zhang X, Zhu W, et al. Novel avian influenza A(H7N9) virus in tree sparrow, Shanghai, China, 2013. Emerg Infect Dis. 2014;20(5):850-3.
- Watanabe T, Kiso M, Fukuyama S, et al. Characterization of H7N9 influenza A viruses isolated from humans. 2013;501(7468):551-5.
- Xiong X, Martin S, Haire LF, et al. Receptor binding by an H7N9 influenza virus from humans. Nature. 2013;499(7459):496-9.
- Tharakaraman K, Jayaraman A, Raman R, et al. Glycan receptor binding of the influenza A virusH7N9 hemagglutinin. Cell. 2013;153(7):1486-93.
- World Health Organization. Analysis of recent scientific information on avian influenza A(H7N9) virus. 10 February 2017
- World Health Organization. Antigenic and genetic characteristics of zoonotic influenza viruses and development of candidate vaccine viruses for pandemic preparedness. March 2017
図1.鳥インフルエンザA(H7N9)ウイルスのヒトへの感染例 n=1557(7月24日現在, 文献1から引用)
図2.中国本土からの鳥インフルエンザA(H7N9)報告地域 2013年2月~2017年(n=1220, 文献4から引用)
図3.中国本土の鳥インフルエンザA(H7N9)ヒト患者とトリ・環境中の陽性例の報告地域 2015年10月~2017年7月26日(文献21から引用)