お知らせ
感染症情報
研究・検査・病原体管理
サーベイランス
刊行・マニュアル・基準
- 詳細
SARS-CoV-2 Omicron-neutralizing memory B-cells are elicited by two doses of BNT162b2 mRNA vaccine
Ryutaro Kotaki†, Yu Adachi†, Saya Moriyama†, Taishi Onodera†, Shuetsu Fukushi, Takaki Nagakura, Keisuke Tonouchi, Kazutaka Terahara, Lin Sun, Tomohiro Takano, Ayae Nishiyama, Masaharu Shinkai, Kunihiro Oba, Fukumi Nakamura-Uchiyama, Hidefumi Shimizu, Tadaki Suzuki, Takayuki Matsumura, Masanori Isogawa, Yoshimasa Takahashi († These authors contributed equally)
Science Immunology (2022), DOI: 10.1126/sciimmunol.abn8590
mRNAワクチン2回接種後に、オミクロン株に対して中和活性を有する抗体が記憶B細胞に保存されていることを見出しました。今回の発見により、3回接種やブレークスルー感染によってオミクロン中和活性をもつ抗体が血液中に産生されるメカニズムの解明につながることが期待されます。
オミクロン株は多くのアミノ酸変異によりmRNAワクチン2回接種後に誘導される血液抗体から強く逃避しますが、3回接種やブレークスルー感染後の血液にはオミクロン中和抗体が誘導されることが報告されています。本研究では、mRNAワクチン2回接種後に誘導された記憶B細胞を取り出し、この細胞に保存されている抗体を解析しました。すると、中和活性をもつ抗体のうち、約30%の抗体がオミクロン株への中和活性を保持していることを明らかとしました。ワクチン3回接種やブレークスルー感染後には、これら記憶B細胞が反応してオミクロン株に対する中和抗体を血液中に産生する可能性が示唆されます。
本内容はAMEDの研究支援を受けて実施しました。
続きを読む: SARS-CoV-2オミクロン株を中和する記憶B細胞はBNT162b2 mRNAワクチンの2回接種により誘導される
- 詳細
Dasabuvir Inhibits Human Norovirus Infection in Human Intestinal Enteroids
Tsuyoshi Hayashi, Kosuke Murakami, Junki Hirano, Yoshiki Fujii, Yoko Yamaoka, Hirofumi Ohashi, Koichi Watashi, Mary K Estes, Masamichi Muramatsu
mSphere. 2021 Dec 22;6(6):e0062321.
https://journals.asm.org/doi/10.1128/mSphere.00623-21
doi: 10.1128/mSphere.00623-21.
ヒトノロウイルス (HuNoV) は、嘔吐、下痢などを主症状とするウイルス性の感染性胃腸炎の主要病原体である。公衆衛生上重要な病原体であるが、有効な治療薬・予防薬は存在しない。
我々は、幹細胞から作製した腸管エンテロイドを用い、HuNoVを試験管内で安定的に増殖させる系を確立した。本研究では当該培養系を駆使して、326種の化合物のHuNoV増殖に対する阻害能を評価した。その結果、C型肝炎ウイルス治療薬として開発されたダサブビルがHuNoV増殖を効果的に抑制することを示した。また、当該化合物は、ヒトロタウイルス、および新型コロナウイルスの腸管エンテロイドでの増殖も抑制した。本研究の成果が、今後のHuNoV治療薬開発において重要な知見となることが期待される。
本研究は、JSPSおよびAMEDの研究支援を受けて実施された。
- 詳細
A lethal mouse model for evaluating vaccine-associated enhanced respiratory disease during SARS-CoV-2 infection
Iwata-Yoshikawa N, Shiwa N, Sekizuka T, Sano K, Ainai A, Hemmi T, Kataoka M, Kuroda M, Hasegawa H, Suzuki T, Nagata N
Science Advances Volume 8, Issue 1, January 2022
COVID-19のワクチン開発における安全上の懸念の1つに「ワクチン関連呼吸器疾患増強現象」が挙げられますが、これは感染動物モデルにおいて好酸球性の免疫病理として特徴付けられており、Th2に偏った免疫応答と感染防御に不十分な中和抗体誘導に起因するとされています。今回研究グループは、SARS-CoV-2マウス継代株を用いて、感染動物モデルを確立し、新規ワクチンの有効性とワクチン関連呼吸器疾患増強現象のリスクを検証するための新しい評価系を開発いたしました。近交系マウスを用いるこの評価系の利点としては、免疫から感染に至る一連の宿主応答に関するTh1/Th2バランス等の免疫学的評価、SARS-CoV-2抗原特異的抗体価と中和抗体価等の評価を容易にし、さらに、感染後の疾患増強のリスク評価が可能となったことが挙げられます。よって、この感染動物モデルは現在までに進められてきたCOVID-19ワクチン開発において、その設計思想が正しいことを証明するだけでなく、さらには安全性の高い次世代COVID-19ワクチン開発や新規治療法開発、COVID-19の病態を理解する上で新しい知見をもたらすことが期待されます。
本研究は、AMEDの研究支援を受けて実施いたしました。
- 詳細
MARCH8 targets cytoplasmic lysine residues of various viral envelope glycoproteins
Yanzhao Zhang, Seiya Ozono, Takuya Tada, Minoru Tobiume, Masanori Kameoka, Satoshi Kishigami, Hideaki Fujita, and Kenzo Tokunaga.
Microbiol Spectr. 2022 Jan 12:e0061821.
https://journals.asm.org/doi/10.1128/spectrum.00618-21
DOI: 10.1128/spectrum.00618-21
我々は以前、宿主膜蛋白質MARCH8が水胞性口炎ウイルスGおよびHIV-1エンベロープのウイルス粒子への取込みを阻害する抗ウイルス宿主因子であることを報告した(Nature Medicine, 21:1502-7. 2015, eLife, 9:e57763, 2020)が、今回、様々なウイルスエンベロープ糖蛋白質に対するMARCH8の抗ウイルス活性を検討した。狂犬病ウイルスG、リンパ球性脈絡髄膜炎ウイルスGP、SARSコロナウイルス及び新型コロナウイルスのスパイク、ロスリバーウイルス及びチクングニアウイルスE2の各細胞質領域にあるリジン残基が、MARCH8の標的となってユビキチン化され、ダウンレギュレーション後にリソソーム分解されること、さらに一部のウイルスエンベロープ糖蛋白質はMARCH8のチロシンモチーフ依存的にダウンレギュレーションされることを明らかにした。本研究結果はMARCH8が幅広い抗ウイルススペクトラムを有することを示すものである。
- 詳細
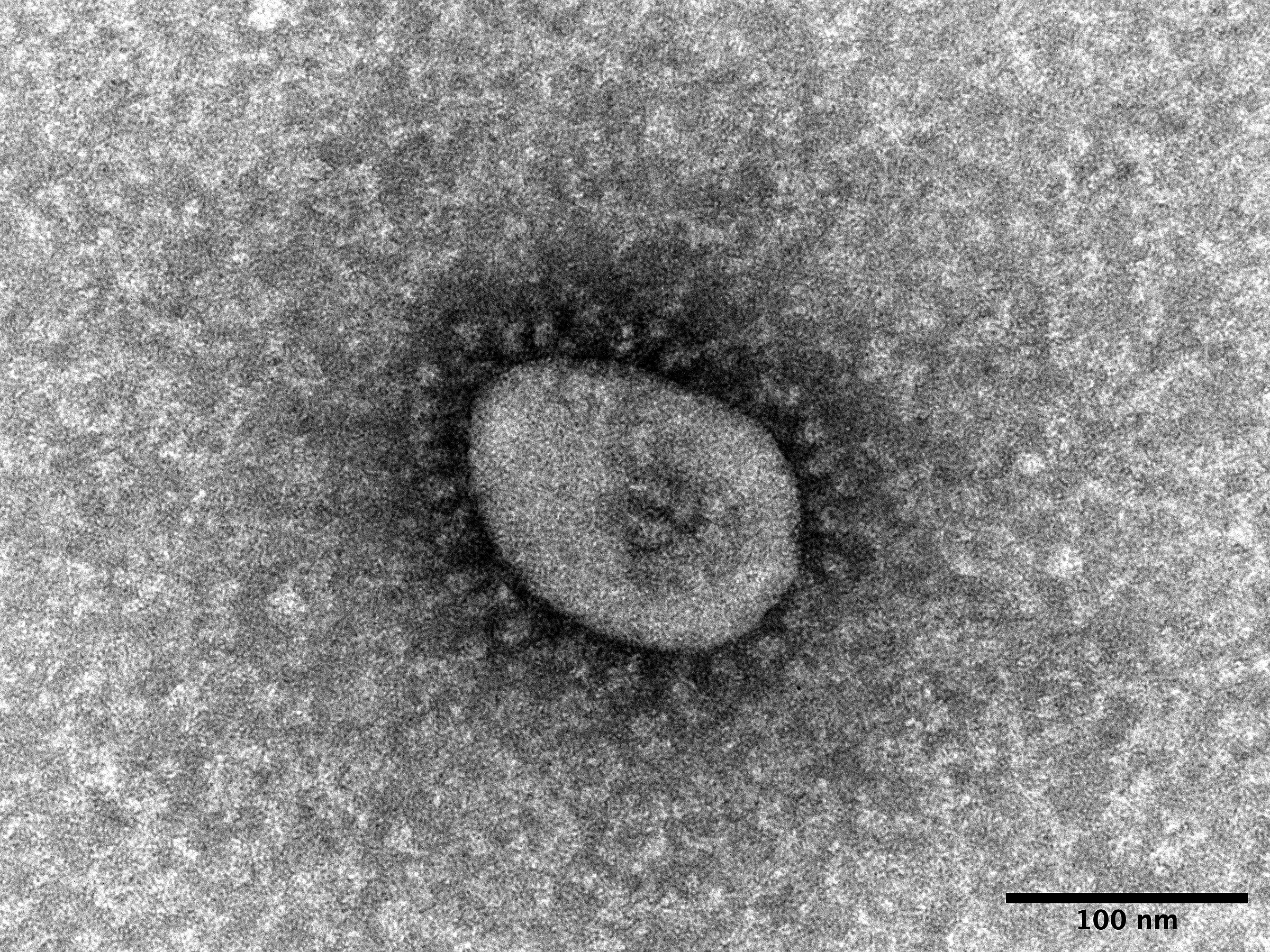
国立感染症研究所において、SARS-CoV-2 B.1.1.529(オミクロン)系統(SARS-CoV-2 Variant of Concern, Lineage B.1.1.529, Omicron)のウイルス分離に成功しました。
※下のサムネイル画像をクリックすると、大きな画像を取得することができます。
- 詳細
Nasal alum-adjuvanted vaccine promotes IL-33 release from alveolar epithelial cells that elicits IgA production via type 2 immune responses
Eita Sasaki, Hideki Asanuma, Haruka Momose, Keiko Furuhata, Takuo Mizukami, Isao Hamaguchi
PLoS Pathog. 2021 Aug 30;17(8):e1009890. doi: 10.1371/journal.ppat.1009890.
アルミニウム塩は、ワクチンの有効性を増強させる”アジュバント”と呼ばれる添加物として、古くから使用されている。しかしながら、粘膜免疫におけるアルミニウム塩による自然免疫活性化機構は十分に明らかにされてこなかった。
本成果では、経鼻接種ワクチンでアルミニウム塩が自然免疫を活性化する新しい分子機構として,肺胞上皮細胞の細胞死によって放出されるインターロイキン (IL)-33を介した免疫制御機構を見い出した。放出されたIL-33は、2型自然リンパ球や抗原提示細胞の活性化などにより、抗原特異的なIgA抗体産生を誘導することが明らかになった。これらの成果は、IL-33が経鼻ワクチンにおけるアジュバント作用に重要であることを示しており、今後のアジュバント設計における重要な知見となりうると考えられる。
続きを読む: アルミニウム塩アジュバント含有経鼻ワクチンは肺胞上皮細胞からのIL-33分泌を促し、2型免疫応答によるIgA抗体産生を促進させる